Gratis (1) 30 ml bacteriostatisch water
met gekwalificeerde bestellingen over$ 500 USD.
(sluit capsuleproducten, cosmetische peptiden, promotiecodes en verzending uit)
Wat is LL-37 (CAP-18)?
LL-37 structuur

LL-37 onderzoek
LL-37 en ontstekingsziekten
LL-37, hoewel voornamelijk gefactureerd als een antimicrobieel peptide, speelt eigenlijk een rol bij een aantal inflammatoire ziekten zoals psoriasis, lupus, reumatoïde artritis en atherosclerose. Afhankelijk van de lokale ontstekingsomgeving en de specifieke cellen, heeft LL-37 verschillende modulerend gedrag van het immuunsysteem. Het is gevonden om:- decrease keratinocyte apoptosis,
- increase IFN-alpha production,
- alter chemotaxis of neutrophils and eosinophils,
- down-regulate signaling through toll-like receptor 4 (TLR4),
- verhoog de productie van IL-18, en
- Verlaag niveaus van atherosclerotische plaques[1].
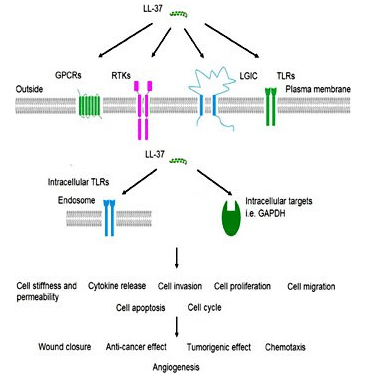
LL-37 is een krachtige antimicrobiële
LL-37 maakt deel uit van het aangeboren immuunsysteem en is als zodanig een van de eerste stukken van het immuunsysteem dat tijdens infectie wordt geactiveerd. Onderzoek bij huidinfecties suggereert dat de normale huid zeer lage niveaus van LL-37 heeft, maar dat het peptide zich snel ophoopt in aanwezigheid van binnenvallende pathogenen. Het is aangetoond dat het peptide samenwerkt met andere eiwitten, zoals menselijke bèta-defensine 2 om infectie te bestrijden[3]. LL-37 primarily works by binding to bacterial lipopolysaccharide (LPS), a major component of the outer membrane of gram-negative bacteria. LPS is a critical component of membrane integrity in these bacteria. The ability of LL-37 to bind to and interfere with LPS means it is exceptionally deadly to certain bacteria. There is interest in using the peptide exogenously to treat serious bacterial infections in people[4]. Despite the fact that LL-37 acts on the cell membrane components of gram-negative bacteria, it still has potent gram-positive effects as well. This could make it a beneficial treatment for staph infections and other serious bacteria. In vitro research indicates that LL-37 enhances the effects of lysozyme, an enzyme responsible for the destruction of gram positive bacteria like Staph aureus[5].LL-37 en longziekte
LPS, zoals hierboven vermeld, is niet uniek voor bacteriële celwanden. Het wordt gevonden in een aantal verschillende organismen en wordt in sommige gevallen in de lucht wanneer een omgeving is besmet door schimmel of andere schimmels. Wanneer LPS wordt ingeademd, reageert het normale longweefsel door te produceren. Helaas is de reactie vaak onvoldoende om het toxische stofsyndroom te voorkomen en de pathogenese van luchtwegaandoeningen zoals astma, COPD en meer. Onderzoek naar het gebruik van LL-37 als een ingeademde behandeling voor het toxische stofsyndroom is momenteel aan de gang[6]. One of the interesting findings of research into the effects of LL-37 on lung disease is that the peptide promotes epithelial cell proliferation and wound closure. It appears that one of the primary properties of LL-37, at least in the lungs, is to attract airway epithelial cells to the site of injury and promote both wound healing and the growth of blood vessels necessary for providing nutrients to the new tissue. It seems that LL-37 is an important homeostatic regulator in the airways just as it has been found to be a homeostatic regulator of immune function[7].Inzicht in LL-37 bij artritis
Onderzoek bij ratten geeft aan dat LL-37 wordt gevonden in hoge concentraties in gewrichten die worden beïnvloed door reumatoïde artritis. In het bijzonder lijkt het peptide geassocieerd te zijn met de pathologische gebeurtenissen van artritis. Het is echter niet duidelijk als het peptide oorzakelijk is of de opregulatie ervan in deze gewrichten is een onderdeel van de poging van het lichaam om het pathologische proces te beheersen[8]. Several things, however, suggest that LL-37 is beneficial in inflammation and not causative. First, there is no evidence that LL-37 or any other cathelicidin is involved in the pathogenesis of inflammatory disease. This does not rule the peptide out as being causative, the but evidence weighs pretty heavily against that being the case. In particular, LL-37 deficiency does not affect outcomes in animal models of arthritis or lupus. In other words, animals without LL-37 experience the same pathological progression as animals who have the peptide. Based on these findings, scientists have suggested that reactivity against cathelicidins in arthritis is likely an epiphenomenon that results from extensive over-expression of the peptide in inflamed tissues[9]. In other words, it is incidental. Research in mouse models of arthritis indicate that peptides derived from LL-37 confer protection against collagen damage that often occurs in inflammatory arthritis. Administration of these peptides directly to affected joints decreases the severity of disease as well as serum levels of antibody against type II collagens[10]. Op basis van deze studie is het redelijk om te speculeren dat LL-37 waarschijnlijk beschermende activiteit heeft bij artritis, wat de hoge concentraties in weefsels met aanzienlijke ontsteking zou kunnen verklaren. Deze speculatie wordt ondersteund door het feit dat is aangetoond dat LL-37 en zijn derivaten ontstekingen reguleren veroorzaakt door interleukine-32, een molecuul dat direct is geassocieerd met de ernst van inflammatoire artritis[11]. Arthritis has also been associated with an up-regulation of toll-like receptor 3 in the fibroblasts of synovial fluid, a factor that likely aggravates arthritis by increasing inflammatory cytokine levels[12]. Het is aangetoond dat LL-37 bindt aan TLR4 en ofwel pro-inflammatoire of ontstekingsremmende effecten bevorderen. Wat het doet in de setting van TLR3-opregulatie is niet duidelijk, maar onderzoek is aan de gang. Het idee dat het selectief ontstekingen kan verminderen, is niet onredelijk, aangezien LL-37 is gevonden om selectief pro-inflammatoire macrofaagreacties in het verleden te verminderen[13].LL-37 en de darm
Onderzoek in celculturen geeft aan dat LL-37 verschillende effecten heeft in de darm. Ten eerste verhoogt het peptide de migratie van cellen die nodig zijn voor het handhaven van de epitheliale barrière van de darm. Ten tweede vermindert LL-37 apoptose in de setting van darmontsteking, waardoor de pathogenese van een aantal inflammatoire aandoeningen wordt vertragen. Over het algemeen geeft het onderzoek aan dat LL-37 een nuttige adjuvante behandeling kan zijn in inflammatoire darmaandoeningen, na darmchirurgie of in de setting van acute darminfecties. Het kan zelfs nuttig blijken te zijn als adjuvans voor antibioticatherapie, waardoor de GI -bijwerkingen worden voorkomen die vaak het oraal antibioticagebruik beperken[14]. LL-37 does not work alone in the intestine, pairing once again with human beta defensin 2 to promote wound healing. Research in cell culture indicates that the peptides work in tandem to both repair and maintain intestinal epithelium while reducing TNF-related cell death[15]. Momenteel zijn TNF-alfa-remmers een steunpilaar van de behandeling voor inflammatoire darmaandoeningen. Ze zijn effectieve medicijnen, maar hebben een aantal ernstige bijwerkingen, waaronder het veroorzaken van een drastische toename van het risico op ernstige infectie, zoals tuberculose. De ontwikkeling van op LL-37 gebaseerde behandelingen van inflammatoire darmaandoeningen zou kunnen helpen de afhankelijkheid van TNF-alfa-remmers te verminderen en de morbiditeit en mortaliteit bij deze patiëntenpopulatie te verbeteren.LL-37 en darmkanker
Onderzoek met betrekking tot LL-37 en kanker heeft gemengde resultaten opgeleverd, maar het peptide lijkt gunstig te zijn in de setting van darm- en maagkankers, waaronder orale plaveiselcelcarcinoom geassocieerd met roken en tabaksgebruik. Interessant is dat deze effecten lijken te worden gemedieerd door een vitamine-D-afhankelijke route, wat kan verklaren waarom het nemen van de vitamine eerder is geassocieerd met een verminderd risico op GI-kanker. Het lijkt erop dat vitamine D de anti-kankeractiviteit van tumor-geassocieerde macrofagen induceert via LL-37[16].LL-37 en de groei van het bloedvat
LL-37 lijkt de synthese van prostaglandine E2 (PGE2) in endotheelcellen te activeren. PGE2 wordt geassocieerd met zowel inflammatoire pijn als met de groei van bloedvaten, maar deze effecten verschillen op basis van waar het molecuul wordt uitgedrukt. In endotheelcellen activeert PGE2 de ontwikkeling van bloedvaten in een proces dat angiogenese wordt genoemd[17]. Dit kan zowel goed als slecht zijn, afhankelijk van de specifieke instelling. Het vermogen om angiogenese te reguleren is de focus geweest van veel onderzoek in de afgelopen decennia omdat het van invloed is op de ontwikkeling van kanker, hartaandoeningen, uitkomsten van beroertes, wondgenezing en meer. LL-37-activiteit biedt een nuttig middel om de angiogenese-route te onderzoeken, evenals een model voor potentiële toekomstige interventies om zowel de groei van het bloedvat te bevorderen wanneer dat nodig is (bijvoorbeeld hartaandoeningen) en het ontmoedigen wanneer het schadelijk is (bijvoorbeeld kanker).Lopend LL-37 onderzoek
Artikelauteur
Wetenschappelijke tijdschrift Auteur
Vermeld citaten
- J. M. Kahlenberg and M. J. Kaplan, “Little peptide, big effects: the role of LL-37 in inflammation and autoimmune disease,” J. Immunol. Baltim. Md 1950, vol. 191, no. 10, Nov. 2013.
D. S. Alexandre-Ramos et al., “LL-37 treatment on human peripheral blood mononuclear cells modulates immune response and promotes regulatory T-cells generation,” Biomed. Pharmacother. Biomedecine Pharmacother., vol. 108, pp. 1584–1590, Dec. 2018.
P. Y. Ong et al., “Endogenous antimicrobial peptides and skin infections in atopic dermatitis,” N. Engl. J. Med., vol. 347, no. 15, pp. 1151–1160, Oct. 2002.
C. D. Ciornei, T. Sigurdardóttir, A. Schmidtchen, and M. Bodelsson, “Antimicrobial and chemoattractant activity, lipopolysaccharide neutralization, cytotoxicity, and inhibition by serum of analogs of human cathelicidin LL-37,” Antimicrob. Agents Chemother., vol. 49, no. 7, pp. 2845–2850, Jul. 2005.
X. Chen et al., “Synergistic effect of antibacterial agents human β-defensins, cathelicidin LL-37 and lysozyme against Staphylococcus aureus and Escherichia coli,” J. Dermatol. Sci., vol. 40, no. 2, pp. 123–132, Nov. 2005.
M. Golec, “Cathelicidin LL-37: LPS-neutralizing, pleiotropic peptide,” Ann. Agric. Environ. Med. AAEM, vol. 14, no. 1, pp. 1–4, 2007.
R. Shaykhiev et al., “Human endogenous antibiotic LL-37 stimulates airway epithelial cell proliferation and wound closure,” Am. J. Physiol. Lung Cell. Mol. Physiol., vol. 789, no. 5, pp. L842-848, Nov. 2005.
M. H. Hoffmann et al., “The cathelicidins LL-37 and rCRAMP are associated with pathogenic events of arthritis in humans and rats,” Ann. Rheum. Dis., vol. 72, no. 7, pp. 1239–1248, Jul. 2013.
D. Kienhöfer et al., “No evidence of pathogenic involvement of cathelicidins in patient cohorts and mouse models of lupus and arthritis,” PloS One, vol. 9, no. 12, p. e115474, 2014.
L. N. Y. Chow et al., “Human cathelicidin LL-37-derived peptide IG-19 confers protection in a murine model of collagen-induced arthritis,” Mol. Immunol., vol. 57, no. 2, pp. 86–92, Feb. 2014.
K.-Y. G. Choi, S. Napper, and N. Mookherjee, “Human cathelicidin LL-37 and its derivative IG-19 regulate interleukin-32-induced inflammation,” Immunology, vol. 143, no. 1, pp. 68–80, Sep. 2014.
W. Zhu et al., “Arthritis is associated with T-cell-induced upregulation of Toll-like receptor 3 on synovial fibroblasts,” Arthritis Res. Ther., vol. 13, no. 3, p. R103, Jun. 2011.
K. L. Brown et al., “Host defense peptide LL-37 selectively reduces proinflammatory macrophage responses,” J. Immunol. Baltim. Md 1950, vol. 186, no. 9, pp. 5497–5505, May 2011.
J.-M. Otte et al., “Effects of the cathelicidin LL-37 on intestinal epithelial barrier integrity,” Regul. Pept., vol. 156, no. 1–3, pp. 104–117, Aug. 2009.
J.-M. Otte et al., “Human beta defensin 2 promotes intestinal wound healing in vitro,” J. Cell. Biochem., vol. 104, no. 6, pp. 2286–2297, Aug. 2008.
X. Chen et al., “Roles and Mechanisms of Human Cathelicidin LL-37 in Cancer,” Cell. Physiol. Biochem. Int. J. Exp. Cell. Physiol. Biochem. Pharmacol., vol. 47, no. 3, pp. 1060–1073, 2018.
Salvado M. Dolores, Di Gennaro Antonio, Lindbom Lennart, Agerberth Birgitta, and Haeggström Jesper Z., “Cathelicidin LL-37 Induces Angiogenesis via PGE2–EP3 Signaling in Endothelial Cells, In Vivo Inhibition by Aspirin,” Arterioscler. Thromb. Vasc. Biol., vol. 33, no. 8, pp. 1965–1972, Aug. 2013.
D. Xhindoli, S. Pacor, M. Benincasa, M. Scocchi, R. Gennaro, and A. Tossi, “The human cathelicidin LL-37 — A pore-forming antibacterial peptide and host-cell modulator,” Biochim. Biophys. Acta BBA – Biomembr., vol. 1858, no. 3, pp. 546–566, Mar. 2016.