Gratis (1) 30 ml de agua bacteriostática
con pedidos calificados sobre$500USD.
(excluye productos en cápsulas, péptidos cosméticos, códigos promocionales y envío)
¿Qué es LL-37 (CAP-18)?
Estructura LL-37

Investigación LL-37
LL-37 y Enfermedades Inflamatorias
El LL-37, aunque se anuncia principalmente como un péptido antimicrobiano, en realidad desempeña un papel en una serie de enfermedades inflamatorias como la psoriasis, el lupus, la artritis reumatoide y la aterosclerosis. Dependiendo del entorno inflamatorio local y de las células particulares involucradas, LL-37 tiene varios comportamientos moduladores del sistema inmunológico diferentes. Se ha descubierto que:- decrease keratinocyte apoptosis,
- increase IFN-alpha production,
- alter chemotaxis of neutrophils and eosinophils,
- down-regulate signaling through toll-like receptor 4 (TLR4),
- aumentar la producción de IL-18, y
- disminuir los niveles de placas ateroscleróticas[1].
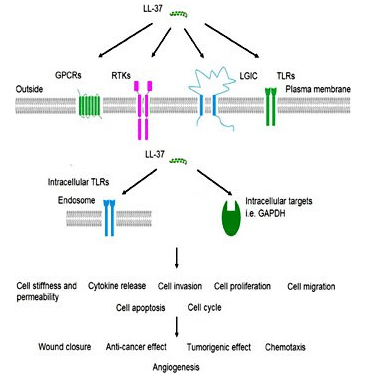
LL-37 es un potente antimicrobiano
LL-37 es parte del sistema inmunológico innato y, como tal, es una de las primeras partes del sistema inmunológico que se activa durante la infección. La investigación sobre infecciones de la piel sugiere que la piel normal tiene niveles muy bajos de LL-37 pero que el péptido se acumula rápidamente en presencia de patógenos invasores. Se ha demostrado que el péptido funciona en conjunto con otras proteínas, como la beta-defensina 2 humana, para combatir infecciones.[3]. LL-37 actúa principalmente uniéndose al lipopolisacárido bacteriano (LPS), un componente importante de la membrana externa de las bacterias gramnegativas. El LPS es un componente crítico de la integridad de la membrana de estas bacterias. La capacidad del LL-37 para unirse e interferir con el LPS significa que es excepcionalmente mortal para ciertas bacterias. Existe interés en utilizar el péptido de forma exógena para tratar infecciones bacterianas graves en personas.[4]. A pesar de que LL-37 actúa sobre los componentes de la membrana celular de las bacterias gramnegativas, también tiene potentes efectos grampositivos. Esto podría convertirlo en un tratamiento beneficioso para las infecciones por estafilococos y otras bacterias graves. La investigación in vitro indica que LL-37 potencia los efectos de la lisozima, una enzima responsable de la destrucción de bacterias grampositivas como Staph aureus.[5].LL-37 y enfermedad pulmonar
El LPS, como se mencionó anteriormente, no es exclusivo de las paredes celulares bacterianas. Se encuentra en varios organismos diferentes y, en algunos casos, se transmite por el aire cuando un ambiente está contaminado por moho u otros hongos. Cuando se inhala LPS, el tejido pulmonar normal responde produciendo. Desafortunadamente, la respuesta suele ser inadecuada para prevenir el síndrome del polvo tóxico y la patogénesis de enfermedades respiratorias como el asma, la EPOC y más. Actualmente se están realizando investigaciones sobre el uso de LL-37 como tratamiento inhalado para el síndrome del polvo tóxico.[6]. Uno de los hallazgos interesantes de la investigación sobre los efectos de LL-37 en las enfermedades pulmonares es que el péptido promueve la proliferación de células epiteliales y el cierre de heridas. Parece que una de las propiedades principales de LL-37, al menos en los pulmones, es atraer células epiteliales de las vías respiratorias al sitio de la lesión y promover tanto la curación de heridas como el crecimiento de los vasos sanguíneos necesarios para proporcionar nutrientes al tejido nuevo. Parece que LL-37 es un regulador homeostático importante en las vías respiratorias, del mismo modo que se ha descubierto que es un regulador homeostático de la función inmune.[7].Comprender LL-37 en la artritis
La investigación en ratas indica que LL-37 se encuentra en altas concentraciones en las articulaciones afectadas por la artritis reumatoide. En particular, el péptido parece estar asociado con los acontecimientos patológicos de la artritis. Sin embargo, no está claro si el péptido es la causa o si su regulación positiva en estas articulaciones es parte del intento del cuerpo de controlar el proceso patológico.[8]. Sin embargo, varias cosas sugieren que LL-37 es beneficioso para la inflamación y no causativo. En primer lugar, no hay evidencia de que LL-37 o cualquier otra catelicidina esté implicada en la patogénesis de la enfermedad inflamatoria. Esto no descarta que el péptido sea la causa, pero la evidencia pesa bastante en contra de que ese sea el caso. En particular, la deficiencia de LL-37 no afecta los resultados en modelos animales de artritis o lupus. En otras palabras, los animales sin LL-37 experimentan la misma progresión patológica que los animales que tienen el péptido. Con base en estos hallazgos, los científicos han sugerido que la reactividad contra las catelicidinas en la artritis es probablemente un epifenómeno que resulta de una sobreexpresión extensa del péptido en los tejidos inflamados.[9]. En otras palabras, es incidental. La investigación en modelos de artritis en ratones indica que los péptidos derivados de LL-37 confieren protección contra el daño del colágeno que a menudo ocurre en la artritis inflamatoria. La administración de estos péptidos directamente a las articulaciones afectadas disminuye la gravedad de la enfermedad, así como los niveles séricos de anticuerpos contra los colágenos tipo II.[10]. Con base en este estudio, es razonable especular que LL-37 probablemente tenga actividad protectora en la artritis, lo que podría explicar sus altas concentraciones en tejidos con inflamación sustancial. Esta especulación está respaldada por el hecho de que se ha demostrado que LL-37 y sus derivados regulan la inflamación causada por la interleucina-32, una molécula que se ha asociado directamente con la gravedad de la artritis inflamatoria.[11]. La artritis también se ha asociado con una regulación positiva del receptor tipo peaje 3 en los fibroblastos del líquido sinovial, un factor que probablemente agrava la artritis al aumentar los niveles de citoquinas inflamatorias.[12]. Se ha demostrado que LL-37 se une a TLR4 y promueve efectos proinflamatorios o antiinflamatorios. No está claro qué hace en el contexto de la regulación positiva de TLR3, pero se están realizando investigaciones. La idea de que podría reducir la inflamación de forma selectiva no es descabellada dado que en el pasado se ha descubierto que LL-37 reduce selectivamente las respuestas proinflamatorias de los macrófagos.[13].LL-37 y el intestino
La investigación en cultivos celulares indica que LL-37 tiene varios efectos en el intestino. En primer lugar, el péptido aumenta la migración de células necesarias para mantener la barrera epitelial del intestino. En segundo lugar, LL-37 reduce la apoptosis en el contexto de inflamación intestinal, lo que ayuda a retardar la patogénesis de una serie de afecciones inflamatorias. En general, la investigación indica que LL-37 puede ser un tratamiento adyuvante útil en afecciones inflamatorias del intestino, después de una cirugía intestinal o en el contexto de infecciones intestinales agudas. Incluso puede resultar útil como coadyuvante de la terapia con antibióticos, ayudando a prevenir los efectos secundarios gastrointestinales que a menudo limitan el uso de antibióticos orales.[14]. LL-37 no funciona solo en el intestino, sino que se combina una vez más con la beta defensina 2 humana para promover la cicatrización de heridas. La investigación en cultivos celulares indica que los péptidos trabajan en conjunto para reparar y mantener el epitelio intestinal mientras reducen la muerte celular relacionada con el TNF.[15]. Actualmente, los inhibidores del TNF-alfa son la base del tratamiento de las enfermedades inflamatorias del intestino. Son medicamentos eficaces, pero tienen una serie de efectos secundarios graves, incluido un aumento drástico del riesgo de infecciones graves, como la tuberculosis. El desarrollo de tratamientos para la enfermedad inflamatoria intestinal basados en LL-37 podría ayudar a reducir la dependencia de los inhibidores del TNF-alfa y mejorar la morbilidad y la mortalidad en esta población de pacientes.LL-37 y cáncer intestinal
La investigación sobre LL-37 y el cáncer ha producido resultados mixtos, pero el péptido parece ser beneficioso en el contexto de cánceres intestinales y gástricos, incluido el carcinoma oral de células escamosas asociado con el tabaquismo y el consumo de tabaco. Curiosamente, estos efectos parecen estar mediados por una vía dependiente de la vitamina D, lo que puede explicar por qué la ingesta de vitamina se ha asociado anteriormente con un riesgo reducido de cáncer gastrointestinal. Parece que la vitamina D induce la actividad anticancerígena de los macrófagos asociados a tumores a través de LL-37[16].LL-37 y crecimiento de vasos sanguíneos
LL-37 parece desencadenar la síntesis de prostaglandina E2 (PGE2) en las células endoteliales. La PGE2 se asocia tanto con el dolor inflamatorio como con el crecimiento de los vasos sanguíneos, pero estos efectos difieren según el lugar donde se expresa la molécula. En las células endoteliales, la PGE2 desencadena el desarrollo de vasos sanguíneos en un proceso llamado angiogénesis.[17]. Esto puede ser tanto bueno como malo, dependiendo del entorno particular. La capacidad de regular la angiogénesis ha sido el foco de muchas investigaciones en las últimas décadas porque afecta el desarrollo del cáncer, las enfermedades cardíacas, los resultados de los accidentes cerebrovasculares, la cicatrización de heridas y más. La actividad de LL-37 ofrece un medio útil para investigar la vía de la angiogénesis, así como un modelo para posibles intervenciones futuras para promover el crecimiento de los vasos sanguíneos cuando sea necesario (por ejemplo, enfermedades cardíacas) y desalentarlo cuando sea perjudicial (por ejemplo, cáncer).Investigación en curso sobre LL-37
Autor del artículo
Autor de revista científica
Citas referenciadas
- J. M. Kahlenberg and M. J. Kaplan, “Little peptide, big effects: the role of LL-37 in inflammation and autoimmune disease,” J. Immunol. Baltim. Md 1950, vol. 191, no. 10, Nov. 2013.
D. S. Alexandre-Ramos et al., “LL-37 treatment on human peripheral blood mononuclear cells modulates immune response and promotes regulatory T-cells generation,” Biomed. Pharmacother. Biomedecine Pharmacother., vol. 108, pp. 1584–1590, Dec. 2018.
P. Y. Ong et al., “Endogenous antimicrobial peptides and skin infections in atopic dermatitis,” N. Engl. J. Med., vol. 347, no. 15, pp. 1151–1160, Oct. 2002.
C. D. Ciornei, T. Sigurdardóttir, A. Schmidtchen, and M. Bodelsson, “Antimicrobial and chemoattractant activity, lipopolysaccharide neutralization, cytotoxicity, and inhibition by serum of analogs of human cathelicidin LL-37,” Antimicrob. Agents Chemother., vol. 49, no. 7, pp. 2845–2850, Jul. 2005.
X. Chen et al., “Synergistic effect of antibacterial agents human β-defensins, cathelicidin LL-37 and lysozyme against Staphylococcus aureus and Escherichia coli,” J. Dermatol. Sci., vol. 40, no. 2, pp. 123–132, Nov. 2005.
M. Golec, “Cathelicidin LL-37: LPS-neutralizing, pleiotropic peptide,” Ann. Agric. Environ. Med. AAEM, vol. 14, no. 1, pp. 1–4, 2007.
R. Shaykhiev et al., “Human endogenous antibiotic LL-37 stimulates airway epithelial cell proliferation and wound closure,” Am. J. Physiol. Lung Cell. Mol. Physiol., vol. 789, no. 5, pp. L842-848, Nov. 2005.
M. H. Hoffmann et al., “The cathelicidins LL-37 and rCRAMP are associated with pathogenic events of arthritis in humans and rats,” Ann. Rheum. Dis., vol. 72, no. 7, pp. 1239–1248, Jul. 2013.
D. Kienhöfer et al., “No evidence of pathogenic involvement of cathelicidins in patient cohorts and mouse models of lupus and arthritis,” PloS One, vol. 9, no. 12, p. e115474, 2014.
L. N. Y. Chow et al., “Human cathelicidin LL-37-derived peptide IG-19 confers protection in a murine model of collagen-induced arthritis,” Mol. Immunol., vol. 57, no. 2, pp. 86–92, Feb. 2014.
K.-Y. G. Choi, S. Napper, and N. Mookherjee, “Human cathelicidin LL-37 and its derivative IG-19 regulate interleukin-32-induced inflammation,” Immunology, vol. 143, no. 1, pp. 68–80, Sep. 2014.
W. Zhu et al., “Arthritis is associated with T-cell-induced upregulation of Toll-like receptor 3 on synovial fibroblasts,” Arthritis Res. Ther., vol. 13, no. 3, p. R103, Jun. 2011.
K. L. Brown et al., “Host defense peptide LL-37 selectively reduces proinflammatory macrophage responses,” J. Immunol. Baltim. Md 1950, vol. 186, no. 9, pp. 5497–5505, May 2011.
J.-M. Otte et al., “Effects of the cathelicidin LL-37 on intestinal epithelial barrier integrity,” Regul. Pept., vol. 156, no. 1–3, pp. 104–117, Aug. 2009.
J.-M. Otte et al., “Human beta defensin 2 promotes intestinal wound healing in vitro,” J. Cell. Biochem., vol. 104, no. 6, pp. 2286–2297, Aug. 2008.
X. Chen et al., “Roles and Mechanisms of Human Cathelicidin LL-37 in Cancer,” Cell. Physiol. Biochem. Int. J. Exp. Cell. Physiol. Biochem. Pharmacol., vol. 47, no. 3, pp. 1060–1073, 2018.
Salvado M. Dolores, Di Gennaro Antonio, Lindbom Lennart, Agerberth Birgitta, and Haeggström Jesper Z., “Cathelicidin LL-37 Induces Angiogenesis via PGE2–EP3 Signaling in Endothelial Cells, In Vivo Inhibition by Aspirin,” Arterioscler. Thromb. Vasc. Biol., vol. 33, no. 8, pp. 1965–1972, Aug. 2013.
D. Xhindoli, S. Pacor, M. Benincasa, M. Scocchi, R. Gennaro, and A. Tossi, “The human cathelicidin LL-37 — A pore-forming antibacterial peptide and host-cell modulator,” Biochim. Biophys. Acta BBA – Biomembr., vol. 1858, no. 3, pp. 546–566, Mar. 2016.