Бесплатно (1) 30 мл бактериостатической воды
с квалифицированными заказами более500 долларов США.
(без учета капсульной продукции, косметических пептидов, промокодов и доставки)
Что такое LL-37 (CAP-18)?
Структура LL-37

LL-37 Исследования
LL-37 и воспалительные заболевания
LL-37, первоначально заявленный как антимикробный пептид, на самом деле играет роль в ряде воспалительных заболеваний, таких как псориаз, волчанка, ревматоидный артрит и атеросклероз. В зависимости от местной воспалительной среды и конкретных задействованных клеток LL-37 обладает несколькими различными свойствами модуляции иммунной системы. Было обнаружено:- decrease keratinocyte apoptosis,
- increase IFN-alpha production,
- alter chemotaxis of neutrophils and eosinophils,
- down-regulate signaling through toll-like receptor 4 (TLR4),
- увеличить производство ИЛ-18, и
- снизить уровень атеросклеротических бляшек[1].
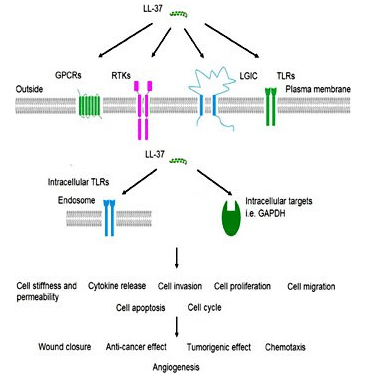
LL-37 — мощный противомикробный препарат.
LL-37 является частью врожденной иммунной системы и, как таковой, является одной из первых частей иммунной системы, которая активируется во время инфекции. Исследования кожных инфекций показывают, что нормальная кожа имеет очень низкий уровень LL-37, но пептид быстро накапливается в присутствии вторгающихся патогенов. Было показано, что пептид работает в тандеме с другими белками, такими как человеческий бета-дефенсин 2, для борьбы с инфекцией.[3]. LL-37 в основном действует путем связывания с бактериальным липополисахаридом (ЛПС), основным компонентом внешней мембраны грамотрицательных бактерий. ЛПС является важнейшим компонентом целостности мембран этих бактерий. Способность LL-37 связываться с ЛПС и вмешиваться в него означает, что он исключительно смертелен для некоторых бактерий. Существует интерес к экзогенному использованию пептида для лечения серьезных бактериальных инфекций у людей.[4]. Несмотря на то, что LL-37 действует на компоненты клеточных мембран грамотрицательных бактерий, он также оказывает мощное действие на грамположительные бактерии. Это может сделать его полезным средством лечения стафилококковых инфекций и других серьезных бактерий. Исследования in vitro показывают, что LL-37 усиливает действие лизоцима, фермента, ответственного за уничтожение грамположительных бактерий, таких как Staph aureus.[5].LL-37 и заболевания легких
ЛПС, как упоминалось выше, не является уникальным для клеточных стенок бактерий. Он обнаруживается в ряде различных организмов и в некоторых случаях передается по воздуху при загрязнении окружающей среды плесенью или другими грибами. При вдыхании ЛПС нормальная легочная ткань реагирует его выработкой. К сожалению, ответных мер часто недостаточно для предотвращения синдрома токсической пыли и патогенеза респираторных заболеваний, таких как астма, ХОБЛ и других. В настоящее время проводятся исследования по использованию LL-37 в качестве ингаляционного средства для лечения синдрома токсической пыли.[6]. Одним из интересных результатов исследований влияния LL-37 на заболевания легких является то, что пептид способствует пролиферации эпителиальных клеток и закрытию ран. Похоже, что одним из основных свойств LL-37, по крайней мере в легких, является привлечение эпителиальных клеток дыхательных путей к месту повреждения и содействие как заживлению ран, так и росту кровеносных сосудов, необходимых для снабжения новой ткани питательными веществами. Похоже, что LL-37 является важным гомеостатическим регулятором дыхательных путей, так же как было обнаружено, что он является гомеостатическим регулятором иммунной функции.[7].Понимание LL-37 при артрите
Исследования на крысах показывают, что LL-37 обнаруживается в высоких концентрациях в суставах, пораженных ревматоидным артритом. В частности, пептид, по-видимому, связан с патологическими явлениями артрита. Однако неясно, является ли пептид причиной или его активация в этих суставах является частью попытки организма контролировать патологический процесс.[8]. Однако некоторые факты позволяют предположить, что LL-37 полезен при воспалении, а не является его причиной. Во-первых, нет никаких доказательств того, что LL-37 или какой-либо другой кателицидин участвует в патогенезе воспалительного заболевания. Это не исключает того, что пептид является причиной заболевания, но доказательства свидетельствуют против этого. В частности, дефицит LL-37 не влияет на исходы на животных моделях артрита или волчанки. Другими словами, у животных без LL-37 наблюдается такое же патологическое прогрессирование, как и у животных, имеющих пептид. Основываясь на этих результатах, ученые предположили, что реактивность против кателицидинов при артрите, вероятно, является эпифеноменом, возникающим в результате чрезмерной экспрессии пептида в воспаленных тканях.[9]. Другими словами, это случайно. Исследования на мышиных моделях артрита показывают, что пептиды, полученные из LL-37, обеспечивают защиту от повреждения коллагена, которое часто возникает при воспалительном артрите. Введение этих пептидов непосредственно в пораженные суставы снижает тяжесть заболевания, а также уровень сывороточных антител против коллагенов II типа.[10]. На основании этого исследования можно предположить, что LL-37, вероятно, обладает защитной активностью при артрите, что может объяснить его высокие концентрации в тканях со значительным воспалением. Это предположение подтверждается тем фактом, что LL-37 и его производные, как было показано, регулируют воспаление, вызванное интерлейкином-32, молекулой, которая напрямую связана с тяжестью воспалительного артрита.[11]. Артрит также связан с усилением регуляции toll-подобного рецептора 3 в фибробластах синовиальной жидкости, фактора, который, вероятно, усугубляет артрит за счет повышения уровня воспалительных цитокинов.[12]. Было показано, что LL-37 связывается с TLR4 и способствует либо провоспалительному, либо противовоспалительному эффекту. Что он делает в условиях повышения регуляции TLR3, неясно, но исследования продолжаются. Идея о том, что он может избирательно уменьшать воспаление, не является необоснованной, учитывая, что в прошлом было обнаружено, что LL-37 избирательно снижает провоспалительные реакции макрофагов.[13].LL-37 и кишечник
Исследования клеточных культур показывают, что LL-37 оказывает несколько эффектов на кишечник. Во-первых, пептид увеличивает миграцию клеток, необходимую для поддержания эпителиального барьера кишечника. Во-вторых, LL-37 снижает апоптоз при воспалении кишечника, помогая замедлить патогенез ряда воспалительных состояний. В целом, исследования показывают, что LL-37 может быть полезным вспомогательным средством при воспалительных заболеваниях кишечника, после операций на кишечнике или при острых кишечных инфекциях. Он может даже оказаться полезным в качестве вспомогательного средства к терапии антибиотиками, помогая предотвратить побочные эффекты со стороны желудочно-кишечного тракта, которые часто ограничивают применение пероральных антибиотиков.[14]. LL-37 не работает в кишечнике в одиночку, он снова соединяется с бета-дефензином 2 человека, способствуя заживлению ран. Исследования в культуре клеток показывают, что пептиды работают в тандеме, восстанавливая и поддерживая кишечный эпителий, одновременно уменьшая гибель клеток, связанную с TNF.[15]. В настоящее время ингибиторы ФНО-альфа являются основой лечения воспалительных заболеваний кишечника. Они являются эффективными лекарствами, но имеют ряд серьезных побочных эффектов, в том числе резко повышают риск серьезных инфекций, таких как туберкулез. Разработка методов лечения воспалительных заболеваний кишечника на основе LL-37 может помочь снизить зависимость от ингибиторов TNF-альфа и улучшить заболеваемость и смертность в этой популяции пациентов.LL-37 и рак кишечника
Исследования относительно LL-37 и рака дали неоднозначные результаты, но пептид, по-видимому, полезен при раке кишечника и желудка, включая плоскоклеточный рак полости рта, связанный с курением и употреблением табака. Интересно, что эти эффекты, по-видимому, опосредованы витамином D-зависимым путем, что может объяснить, почему прием витамина ранее был связан со снижением риска развития рака желудочно-кишечного тракта. Похоже, что витамин D индуцирует противораковую активность опухолеассоциированных макрофагов посредством LL-37.[16].LL-37 и рост кровеносных сосудов
LL-37, по-видимому, запускает синтез простагландина E2 (PGE2) в эндотелиальных клетках. PGE2 связан как с воспалительной болью, так и с ростом кровеносных сосудов, но эти эффекты различаются в зависимости от того, где экспрессируется молекула. В эндотелиальных клетках PGE2 запускает развитие кровеносных сосудов в процессе, называемом ангиогенезом.[17]. Это может быть как хорошо, так и плохо, в зависимости от конкретной ситуации. Способность регулировать ангиогенез была в центре внимания многих исследований в течение последних нескольких десятилетий, поскольку она влияет на развитие рака, болезней сердца, исходы инсульта, заживление ран и многое другое. Активность LL-37 предлагает полезные средства для исследования пути ангиогенеза, а также модель для потенциальных будущих вмешательств, направленных как на стимулирование роста кровеносных сосудов, когда это необходимо (например, при заболеваниях сердца), так и на его подавление, когда это вредно (например, рак).Продолжающиеся исследования LL-37
Автор статьи
Автор научного журнала
Ссылочные цитаты
- J. M. Kahlenberg and M. J. Kaplan, “Little peptide, big effects: the role of LL-37 in inflammation and autoimmune disease,” J. Immunol. Baltim. Md 1950, vol. 191, no. 10, Nov. 2013.
D. S. Alexandre-Ramos et al., “LL-37 treatment on human peripheral blood mononuclear cells modulates immune response and promotes regulatory T-cells generation,” Biomed. Pharmacother. Biomedecine Pharmacother., vol. 108, pp. 1584–1590, Dec. 2018.
P. Y. Ong et al., “Endogenous antimicrobial peptides and skin infections in atopic dermatitis,” N. Engl. J. Med., vol. 347, no. 15, pp. 1151–1160, Oct. 2002.
C. D. Ciornei, T. Sigurdardóttir, A. Schmidtchen, and M. Bodelsson, “Antimicrobial and chemoattractant activity, lipopolysaccharide neutralization, cytotoxicity, and inhibition by serum of analogs of human cathelicidin LL-37,” Antimicrob. Agents Chemother., vol. 49, no. 7, pp. 2845–2850, Jul. 2005.
X. Chen et al., “Synergistic effect of antibacterial agents human β-defensins, cathelicidin LL-37 and lysozyme against Staphylococcus aureus and Escherichia coli,” J. Dermatol. Sci., vol. 40, no. 2, pp. 123–132, Nov. 2005.
M. Golec, “Cathelicidin LL-37: LPS-neutralizing, pleiotropic peptide,” Ann. Agric. Environ. Med. AAEM, vol. 14, no. 1, pp. 1–4, 2007.
R. Shaykhiev et al., “Human endogenous antibiotic LL-37 stimulates airway epithelial cell proliferation and wound closure,” Am. J. Physiol. Lung Cell. Mol. Physiol., vol. 789, no. 5, pp. L842-848, Nov. 2005.
M. H. Hoffmann et al., “The cathelicidins LL-37 and rCRAMP are associated with pathogenic events of arthritis in humans and rats,” Ann. Rheum. Dis., vol. 72, no. 7, pp. 1239–1248, Jul. 2013.
D. Kienhöfer et al., “No evidence of pathogenic involvement of cathelicidins in patient cohorts and mouse models of lupus and arthritis,” PloS One, vol. 9, no. 12, p. e115474, 2014.
L. N. Y. Chow et al., “Human cathelicidin LL-37-derived peptide IG-19 confers protection in a murine model of collagen-induced arthritis,” Mol. Immunol., vol. 57, no. 2, pp. 86–92, Feb. 2014.
K.-Y. G. Choi, S. Napper, and N. Mookherjee, “Human cathelicidin LL-37 and its derivative IG-19 regulate interleukin-32-induced inflammation,” Immunology, vol. 143, no. 1, pp. 68–80, Sep. 2014.
W. Zhu et al., “Arthritis is associated with T-cell-induced upregulation of Toll-like receptor 3 on synovial fibroblasts,” Arthritis Res. Ther., vol. 13, no. 3, p. R103, Jun. 2011.
K. L. Brown et al., “Host defense peptide LL-37 selectively reduces proinflammatory macrophage responses,” J. Immunol. Baltim. Md 1950, vol. 186, no. 9, pp. 5497–5505, May 2011.
J.-M. Otte et al., “Effects of the cathelicidin LL-37 on intestinal epithelial barrier integrity,” Regul. Pept., vol. 156, no. 1–3, pp. 104–117, Aug. 2009.
J.-M. Otte et al., “Human beta defensin 2 promotes intestinal wound healing in vitro,” J. Cell. Biochem., vol. 104, no. 6, pp. 2286–2297, Aug. 2008.
X. Chen et al., “Roles and Mechanisms of Human Cathelicidin LL-37 in Cancer,” Cell. Physiol. Biochem. Int. J. Exp. Cell. Physiol. Biochem. Pharmacol., vol. 47, no. 3, pp. 1060–1073, 2018.
Salvado M. Dolores, Di Gennaro Antonio, Lindbom Lennart, Agerberth Birgitta, and Haeggström Jesper Z., “Cathelicidin LL-37 Induces Angiogenesis via PGE2–EP3 Signaling in Endothelial Cells, In Vivo Inhibition by Aspirin,” Arterioscler. Thromb. Vasc. Biol., vol. 33, no. 8, pp. 1965–1972, Aug. 2013.
D. Xhindoli, S. Pacor, M. Benincasa, M. Scocchi, R. Gennaro, and A. Tossi, “The human cathelicidin LL-37 — A pore-forming antibacterial peptide and host-cell modulator,” Biochim. Biophys. Acta BBA – Biomembr., vol. 1858, no. 3, pp. 546–566, Mar. 2016.