Serbest (1) 30 ml bakteriyostatik su
Nitelikli siparişlerle500 $ USD.
(Kapsül ürünleri, kozmetik peptitler, promosyon kodları ve nakliye hariç)
LL-37 (CAP-18) nedir?
LL-37 yapısı

LL-37 Araştırma
LL-37 ve enflamatuar hastalıklar
LL-37, öncelikle antimikrobiyal bir peptit olarak faturalandırılırken, aslında sedef hastalığı, lupus, romatoid artrit ve ateroskleroz gibi bir dizi enflamatuar hastalıkta rol oynar. Lokal inflamatuar ortama ve ilgili belirli hücrelere bağlı olarak, LL-37'nin birkaç farklı bağışıklık sistemi modülasyon davranışına sahiptir. Şu bulundu:- decrease keratinocyte apoptosis,
- increase IFN-alpha production,
- alter chemotaxis of neutrophils and eosinophils,
- down-regulate signaling through toll-like receptor 4 (TLR4),
- IL-18 üretimini artırın ve
- aterosklerotik plak seviyelerini azaltın[1].
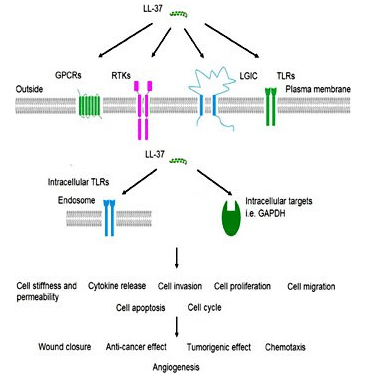
LL-37 güçlü bir antimikrobiyaldir
LL-37, doğuştan gelen bağışıklık sisteminin bir parçasıdır ve bu nedenle enfeksiyon sırasında aktive edilecek bağışıklık sisteminin ilk parçalarından biridir. Cilt enfeksiyonlarında yapılan araştırmalar, normal cildin çok düşük LL-37 seviyelerine sahip olduğunu, ancak peptidin istilacı patojenlerin varlığında hızla biriktiğini göstermektedir. Peptidin, enfeksiyonla mücadele etmek için insan beta-deksensin 2 gibi diğer proteinlerle birlikte çalıştığı gösterilmiştir.[3]. LL-37 primarily works by binding to bacterial lipopolysaccharide (LPS), a major component of the outer membrane of gram-negative bacteria. LPS is a critical component of membrane integrity in these bacteria. The ability of LL-37 to bind to and interfere with LPS means it is exceptionally deadly to certain bacteria. There is interest in using the peptide exogenously to treat serious bacterial infections in people[4]. Despite the fact that LL-37 acts on the cell membrane components of gram-negative bacteria, it still has potent gram-positive effects as well. This could make it a beneficial treatment for staph infections and other serious bacteria. In vitro research indicates that LL-37 enhances the effects of lysozyme, an enzyme responsible for the destruction of gram positive bacteria like Staph aureus[5].LL-37 ve akciğer hastalığı
LPS, yukarıda belirtildiği gibi, bakteriyel hücre duvarlarına özgü değildir. Bir dizi farklı organizmada bulunur ve bazı durumlarda bir ortam küf veya diğer mantarlarla kirlendiğinde havaya uçar. LPS solunduğunda, normal akciğer dokusu üreterek tepki verir. Ne yazık ki, tepki toksik toz sendromunu ve astım, KOAH ve daha fazlası gibi solunum hastalıklarının patogenezini önlemek için genellikle yetersizdir. Toksik toz sendromu için inhale tedavi olarak LL-37'nin kullanımına ilişkin araştırmalar şu anda devam etmektedir.[6]. One of the interesting findings of research into the effects of LL-37 on lung disease is that the peptide promotes epithelial cell proliferation and wound closure. It appears that one of the primary properties of LL-37, at least in the lungs, is to attract airway epithelial cells to the site of injury and promote both wound healing and the growth of blood vessels necessary for providing nutrients to the new tissue. It seems that LL-37 is an important homeostatic regulator in the airways just as it has been found to be a homeostatic regulator of immune function[7].Artritte LL-37'yi anlamak
Sıçanlarda yapılan araştırmalar, Romatoid artritten etkilenen eklemlerde LL-37'nin yüksek konsantrasyonlarda bulunduğunu göstermektedir. Özellikle, peptit artritin patolojik olayları ile ilişkili görünmektedir. Bununla birlikte, peptit nedenselse veya bu eklemlerdeki yukarı regülasyonu, vücudun patolojik süreci kontrol etme girişiminin bir parçasısa açık değildir.[8]. Several things, however, suggest that LL-37 is beneficial in inflammation and not causative. First, there is no evidence that LL-37 or any other cathelicidin is involved in the pathogenesis of inflammatory disease. This does not rule the peptide out as being causative, the but evidence weighs pretty heavily against that being the case. In particular, LL-37 deficiency does not affect outcomes in animal models of arthritis or lupus. In other words, animals without LL-37 experience the same pathological progression as animals who have the peptide. Based on these findings, scientists have suggested that reactivity against cathelicidins in arthritis is likely an epiphenomenon that results from extensive over-expression of the peptide in inflamed tissues[9]. In other words, it is incidental. Research in mouse models of arthritis indicate that peptides derived from LL-37 confer protection against collagen damage that often occurs in inflammatory arthritis. Administration of these peptides directly to affected joints decreases the severity of disease as well as serum levels of antibody against type II collagens[10]. Bu çalışmaya dayanarak, LL-37'nin muhtemelen artritte koruyucu aktiviteye sahip olduğunu tahmin etmek mantıklıdır, bu da önemli iltihaplı dokulardaki yüksek konsantrasyonlarını açıklayabilir. Bu spekülasyon, LL-37 ve türevlerinin, inflamatuar artritin şiddeti ile doğrudan ilişkili bir molekül olan interlökin-32'nin neden olduğu iltihabı düzenlediği gösterilmesiyle desteklenmektedir.[11]. Arthritis has also been associated with an up-regulation of toll-like receptor 3 in the fibroblasts of synovial fluid, a factor that likely aggravates arthritis by increasing inflammatory cytokine levels[12]. LL-37'nin TLR4'e bağlandığı ve pro-enflamatuar veya anti-enflamatuar etkileri desteklediği gösterilmiştir. TLR3 yukarı regülasyonunun ortamında yaptığı açık değildir, ancak araştırma devam etmektedir. Enflamasyonu seçici olarak azaltabileceği fikri, LL-37'nin geçmişte pro-enflamatuar makrofaj yanıtlarını seçici olarak azalttığı düşünüldüğünde mantıksız değildir.[13].LL-37 ve bağırsak
Hücre kültürlerinde yapılan araştırmalar, LL-37'nin bağırsakta çeşitli etkileri olduğunu göstermektedir. İlk olarak, peptit bağırsağın epitel bariyerini korumak için gerekli hücrelerin göçünü arttırır. İkincisi, LL-37, bağırsak inflamasyonu ortamında apoptozu azaltır ve bir dizi inflamatuar durumun patogenezinin yavaşlatılmasına yardımcı olur. Genel olarak, araştırma, LL-37'nin inflamatuar bağırsak koşullarında, bağırsak cerrahisinde veya akut bağırsak enfeksiyonları ortamında yararlı bir adjuvan tedavi olabileceğini göstermektedir. Hatta antibiyotik tedavisine bir adjuvan olarak yararlı olabilir ve genellikle oral antibiyotik kullanımını sınırlayan GI yan etkilerinin önlenmesine yardımcı olabilir.[14]. LL-37 does not work alone in the intestine, pairing once again with human beta defensin 2 to promote wound healing. Research in cell culture indicates that the peptides work in tandem to both repair and maintain intestinal epithelium while reducing TNF-related cell death[15]. Şu anda, TNF-alfa inhibitörleri, inflamatuar bağırsak durumları için bir tedavinin dayanak noktasıdır. Etkili ilaçlardır, ancak tüberküloz gibi ciddi enfeksiyon riskinde ciddi bir artışa neden olmak gibi bir dizi ciddi yan etkiye sahiptirler. Enflamatuar bağırsak hastalığının LL-37 bazlı tedavilerinin gelişimi, TNF-alfa inhibitörlerine olan güveninin azaltılmasına ve bu hasta popülasyonunda morbidite ve mortaliteyi iyileştirmeye yardımcı olabilir.LL-37 ve bağırsak kanseri
LL-37 ve Kanser ile ilgili araştırmalar karışık sonuçlar üretmiştir, ancak peptit, sigara ve tütün kullanımı ile ilişkili oral skuamöz hücreli karsinom da dahil olmak üzere bağırsak ve mide kanserlerinin ortamında yararlı görünmektedir. İlginç bir şekilde, bu etkilere vitamine bağlı bir yol tarafından aracılık ettiği görülmektedir, bu da vitamini almanın neden daha önce GI kanseri riskiyle ilişkili olduğunu açıklayabilir. D vitamininin, LL-37 yoluyla tümörle ilişkili makrofajların anti-kanser aktivitesini indüklediği görülmektedir.[16].LL-37 ve kan damarı büyümesi
LL-37, endotelyal hücrelerde prostaglandin E2 (PGE2) sentezini tetikliyor gibi görünmektedir. PGE2, hem inflamatuar ağrı hem de kan damarlarının büyümesi ile ilişkilidir, ancak bu etkiler molekülün ifade edildiği yere göre farklılık gösterir. Endotelyal hücrelerde, PGE2 anjiyogenez adı verilen bir işlemde kan damarlarının gelişimini tetikler[17]. Bu, belirli ayara bağlı olarak hem iyi hem de kötü olabilir. Anjiyogenezi düzenleme yeteneği, kanser gelişimini, kalp hastalığını, inme sonuçlarını, yara iyileşmesini ve daha fazlasını etkilediği için son birkaç on yılda çok fazla araştırmanın odağı olmuştur. LL-37 aktivitesi, anjiyogenez yolunu araştırmak için yararlı bir araç ve hem gerektiğinde kan damarı büyümesini (örn. Kalp hastalığı) teşvik etmek ve zararlı olduğunda (örn. Kanser) caydırmak için gelecekteki potansiyel müdahaleler için bir model sunmaktadır.Devam eden LL-37 Araştırma
Makale yazarı
Scientific Journal Yazar
Referans alınan alıntılar
- J. M. Kahlenberg and M. J. Kaplan, “Little peptide, big effects: the role of LL-37 in inflammation and autoimmune disease,” J. Immunol. Baltim. Md 1950, vol. 191, no. 10, Nov. 2013.
D. S. Alexandre-Ramos et al., “LL-37 treatment on human peripheral blood mononuclear cells modulates immune response and promotes regulatory T-cells generation,” Biomed. Pharmacother. Biomedecine Pharmacother., vol. 108, pp. 1584–1590, Dec. 2018.
P. Y. Ong et al., “Endogenous antimicrobial peptides and skin infections in atopic dermatitis,” N. Engl. J. Med., vol. 347, no. 15, pp. 1151–1160, Oct. 2002.
C. D. Ciornei, T. Sigurdardóttir, A. Schmidtchen, and M. Bodelsson, “Antimicrobial and chemoattractant activity, lipopolysaccharide neutralization, cytotoxicity, and inhibition by serum of analogs of human cathelicidin LL-37,” Antimicrob. Agents Chemother., vol. 49, no. 7, pp. 2845–2850, Jul. 2005.
X. Chen et al., “Synergistic effect of antibacterial agents human β-defensins, cathelicidin LL-37 and lysozyme against Staphylococcus aureus and Escherichia coli,” J. Dermatol. Sci., vol. 40, no. 2, pp. 123–132, Nov. 2005.
M. Golec, “Cathelicidin LL-37: LPS-neutralizing, pleiotropic peptide,” Ann. Agric. Environ. Med. AAEM, vol. 14, no. 1, pp. 1–4, 2007.
R. Shaykhiev et al., “Human endogenous antibiotic LL-37 stimulates airway epithelial cell proliferation and wound closure,” Am. J. Physiol. Lung Cell. Mol. Physiol., vol. 789, no. 5, pp. L842-848, Nov. 2005.
M. H. Hoffmann et al., “The cathelicidins LL-37 and rCRAMP are associated with pathogenic events of arthritis in humans and rats,” Ann. Rheum. Dis., vol. 72, no. 7, pp. 1239–1248, Jul. 2013.
D. Kienhöfer et al., “No evidence of pathogenic involvement of cathelicidins in patient cohorts and mouse models of lupus and arthritis,” PloS One, vol. 9, no. 12, p. e115474, 2014.
L. N. Y. Chow et al., “Human cathelicidin LL-37-derived peptide IG-19 confers protection in a murine model of collagen-induced arthritis,” Mol. Immunol., vol. 57, no. 2, pp. 86–92, Feb. 2014.
K.-Y. G. Choi, S. Napper, and N. Mookherjee, “Human cathelicidin LL-37 and its derivative IG-19 regulate interleukin-32-induced inflammation,” Immunology, vol. 143, no. 1, pp. 68–80, Sep. 2014.
W. Zhu et al., “Arthritis is associated with T-cell-induced upregulation of Toll-like receptor 3 on synovial fibroblasts,” Arthritis Res. Ther., vol. 13, no. 3, p. R103, Jun. 2011.
K. L. Brown et al., “Host defense peptide LL-37 selectively reduces proinflammatory macrophage responses,” J. Immunol. Baltim. Md 1950, vol. 186, no. 9, pp. 5497–5505, May 2011.
J.-M. Otte et al., “Effects of the cathelicidin LL-37 on intestinal epithelial barrier integrity,” Regul. Pept., vol. 156, no. 1–3, pp. 104–117, Aug. 2009.
J.-M. Otte et al., “Human beta defensin 2 promotes intestinal wound healing in vitro,” J. Cell. Biochem., vol. 104, no. 6, pp. 2286–2297, Aug. 2008.
X. Chen et al., “Roles and Mechanisms of Human Cathelicidin LL-37 in Cancer,” Cell. Physiol. Biochem. Int. J. Exp. Cell. Physiol. Biochem. Pharmacol., vol. 47, no. 3, pp. 1060–1073, 2018.
Salvado M. Dolores, Di Gennaro Antonio, Lindbom Lennart, Agerberth Birgitta, and Haeggström Jesper Z., “Cathelicidin LL-37 Induces Angiogenesis via PGE2–EP3 Signaling in Endothelial Cells, In Vivo Inhibition by Aspirin,” Arterioscler. Thromb. Vasc. Biol., vol. 33, no. 8, pp. 1965–1972, Aug. 2013.
D. Xhindoli, S. Pacor, M. Benincasa, M. Scocchi, R. Gennaro, and A. Tossi, “The human cathelicidin LL-37 — A pore-forming antibacterial peptide and host-cell modulator,” Biochim. Biophys. Acta BBA – Biomembr., vol. 1858, no. 3, pp. 546–566, Mar. 2016.