Freies (1) 30 ml bakteriostatisches Wasser
mit qualifizierten Bestellungen über$ 500 USD.
(Ausgeschlossene Kapselprodukte, kosmetische Peptide, Promo -Codes und Versand)
Was ist LL-37 (CAP-18)?
LL-37 Struktur

LL-37 Forschung
LL-37 und entzündliche Erkrankungen
LL-37 spielt zwar hauptsächlich als antimikrobielles Peptid, spielt tatsächlich eine Rolle bei einer Reihe entzündlicher Erkrankungen wie Psoriasis, Lupus, rheumatoider Arthritis und Atherosklerose. Abhängig von der lokalen entzündlichen Umgebung und den beteiligten Zellen hat LL-37 mehrere verschiedene Verhaltensweisen des Immunsystems. Es wurde gefunden:- decrease keratinocyte apoptosis,
- increase IFN-alpha production,
- alter chemotaxis of neutrophils and eosinophils,
- down-regulate signaling through toll-like receptor 4 (TLR4),
- Erhöhen Sie die IL-18-Produktion und
- Verringern Sie die Spiegel an atherosklerotischen Plaques[1].
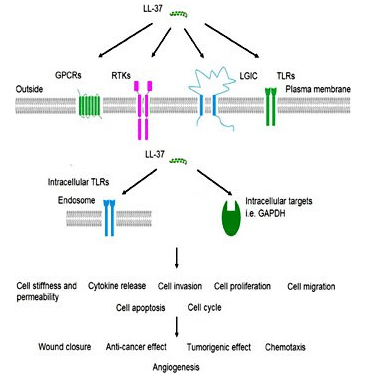
LL-37 ist ein starkes antimikrobielles Antimikrobial
LL-37 ist Teil des angeborenen Immunsystems und als solche eines der ersten Teile des Immunsystems, das während der Infektion aktiviert wird. Untersuchungen bei Hautinfektionen deuten darauf hin, dass normale Haut sehr niedrige LL-37-Spiegel aufweist, sich das Peptid jedoch in Gegenwart von eindringenden Krankheitserregern schnell ansammelt. Es wurde gezeigt, dass das Peptid zusammen mit anderen Proteinen wie menschlicher Beta-Defensin 2 zur Bekämpfung der Infektion funktioniert[3]. LL-37 primarily works by binding to bacterial lipopolysaccharide (LPS), a major component of the outer membrane of gram-negative bacteria. LPS is a critical component of membrane integrity in these bacteria. The ability of LL-37 to bind to and interfere with LPS means it is exceptionally deadly to certain bacteria. There is interest in using the peptide exogenously to treat serious bacterial infections in people[4]. Despite the fact that LL-37 acts on the cell membrane components of gram-negative bacteria, it still has potent gram-positive effects as well. This could make it a beneficial treatment for staph infections and other serious bacteria. In vitro research indicates that LL-37 enhances the effects of lysozyme, an enzyme responsible for the destruction of gram positive bacteria like Staph aureus[5].LL-37 und Lungenerkrankung
LPS ist, wie oben erwähnt, nicht nur für bakterielle Zellwände. Es kommt in einer Reihe verschiedener Organismen vor und wird in einigen Fällen in der Luft, wenn eine Umgebung durch Schimmel oder andere Pilze kontaminiert wird. Wenn LPS eingeatmet wird, reagiert normales Lungengewebe durch Erzeugung. Leider ist die Reaktion oft unzureichend, um das giftige Staubsyndrom und die Pathogenese von Atemwegserkrankungen wie Asthma, COPD und mehr zu verhindern. Die Erforschung der Verwendung von LL-37 als inhalierte Behandlung für toxisches Staubsyndrom ist derzeit im Gange[6]. One of the interesting findings of research into the effects of LL-37 on lung disease is that the peptide promotes epithelial cell proliferation and wound closure. It appears that one of the primary properties of LL-37, at least in the lungs, is to attract airway epithelial cells to the site of injury and promote both wound healing and the growth of blood vessels necessary for providing nutrients to the new tissue. It seems that LL-37 is an important homeostatic regulator in the airways just as it has been found to be a homeostatic regulator of immune function[7].Verständnis LL-37 bei Arthritis
Untersuchungen an Ratten zeigen, dass LL-37 in hohen Konzentrationen in von rheumatoiden Arthritis betroffenen Gelenke festgestellt wird. Insbesondere scheint das Peptid mit den pathologischen Ereignissen der Arthritis verbunden zu sein. Es ist jedoch nicht klar[8]. Several things, however, suggest that LL-37 is beneficial in inflammation and not causative. First, there is no evidence that LL-37 or any other cathelicidin is involved in the pathogenesis of inflammatory disease. This does not rule the peptide out as being causative, the but evidence weighs pretty heavily against that being the case. In particular, LL-37 deficiency does not affect outcomes in animal models of arthritis or lupus. In other words, animals without LL-37 experience the same pathological progression as animals who have the peptide. Based on these findings, scientists have suggested that reactivity against cathelicidins in arthritis is likely an epiphenomenon that results from extensive over-expression of the peptide in inflamed tissues[9]. In other words, it is incidental. Research in mouse models of arthritis indicate that peptides derived from LL-37 confer protection against collagen damage that often occurs in inflammatory arthritis. Administration of these peptides directly to affected joints decreases the severity of disease as well as serum levels of antibody against type II collagens[10]. Basierend auf dieser Studie ist es vernünftig zu spekulieren, dass LL-37 wahrscheinlich eine Schutzaktivität bei Arthritis aufweist, was seine hohen Konzentrationen in Geweben mit erheblicher Entzündung erklären könnte. Diese Spekulation wird durch die Tatsache gestützt, dass LL-37 und seine Derivate nachgewiesen wurden, dass die durch Interleukin-32 verursachte Entzündung reguliert[11]. Arthritis has also been associated with an up-regulation of toll-like receptor 3 in the fibroblasts of synovial fluid, a factor that likely aggravates arthritis by increasing inflammatory cytokine levels[12]. Es wurde gezeigt, dass LL-37 an TLR4 binden und entweder entzündungshemmende oder entzündungshemmende Wirkungen fördern. Was bei der Einstellung von TLR3-Hochregulierung der Fall ist, ist nicht klar, aber die Forschung ist noch nicht abgeschlossen. Die Idee, dass es die Entzündung selektiv verringern könnte, ist nicht unangemessen[13].LL-37 und der Darm
Untersuchungen in Zellkulturen zeigen, dass LL-37 im Darm mehrere Auswirkungen hat. Erstens erhöht das Peptid die Migration von Zellen, die zur Aufrechterhaltung der epithelialen Barriere des Darms erforderlich sind. Zweitens reduziert LL-37 die Apoptose im Aufbau einer Darmentzündung und trägt dazu bei, die Pathogenese einer Reihe entzündlicher Erkrankungen zu verlangsamen. Insgesamt zeigt die Forschung, dass LL-37 eine nützliche adjuvante Behandlung bei entzündlichen Darmerkrankungen, nach Darmoperationen oder bei akuten Darminfektionen sein kann. Es kann sich sogar als Adjuvans gegen Antibiotika -Therapie als nützlich erweisen, was dazu beiträgt, die GI -Nebenwirkungen zu verhindern, die häufig den oralen Antibiotika -Gebrauch einschränken[14]. LL-37 does not work alone in the intestine, pairing once again with human beta defensin 2 to promote wound healing. Research in cell culture indicates that the peptides work in tandem to both repair and maintain intestinal epithelium while reducing TNF-related cell death[15]. Derzeit sind TNF-Alpha-Inhibitoren eine Hauptstütze der Behandlung bei entzündlichen Darmerkrankungen. Sie sind wirksame Medikamente, haben jedoch eine Reihe schwerwiegender Nebenwirkungen, einschließlich eines drastischen Anstiegs des Risikos schwerwiegender Infektionen wie Tuberkulose. Die Entwicklung von LL-37-basierten Behandlungen bei entzündlichen Darmerkrankungen könnte dazu beitragen, die Abhängigkeit von TNF-Alpha-Inhibitoren zu verringern und die Morbidität und Mortalität in dieser Patientenpopulation zu verbessern.LL-37 und Darmkrebs
Untersuchungen zu LL-37 und Krebs haben gemischte Ergebnisse hervorgebracht, aber das Peptid scheint bei Darm- und Magenkrebserkrankungen von Vorteil zu sein, einschließlich orales Plattenepithelkarzinom im Zusammenhang mit Rauchen und Tabakkonsum. Interessanterweise scheinen diese Effekte durch einen Vitamin-D-abhängigen Weg zu vermitteln, was möglicherweise erklären kann, warum das Einnehmen des Vitamins zuvor mit einem verringerten Risiko für GI-Krebs in Verbindung gebracht wurde. Es scheint, dass Vitamin D die Anti-Krebs-Aktivität von tumorassoziierten Makrophagen über LL-37 induziert[16].LL-37 und Blutgefäßwachstum
LL-37 scheint die Synthese von Prostaglandin E2 (PGE2) in Endothelzellen auszulösen. PGE2 ist sowohl mit entzündlichen Schmerzen als auch mit dem Wachstum von Blutgefäßen verbunden, aber diese Effekte unterscheiden sich basierend auf dem Ort, an dem das Molekül exprimiert wird. In Endothelzellen löst PGE2 die Entwicklung von Blutgefäßen in einem Prozess als Angiogenese aus[17]. Dies kann sowohl gut als auch schlecht sein, abhängig von der jeweiligen Einstellung. Die Fähigkeit, die Angiogenese zu regulieren, war in den letzten Jahrzehnten im Mittelpunkt vieler Forschung, da sie sich auf Krebsentwicklung, Herzerkrankungen, Schlaganfallergebnisse, Wundheilung und mehr auswirkt. Die LL-37-Aktivität bietet ein nützliches Mittel zur Untersuchung des Angiogenese-Weges sowie ein Modell für mögliche zukünftige Interventionen, um bei Bedarf das Blutgefäßwachstum zu fördern (z. B. Herzerkrankungen), und es zu entmutigen, wenn es schädlich ist (z. B. Krebs).Laufende LL-37-Forschung
Artikelautor
Autor wissenschaftlicher Zeitschriften
Referenzierte Zitate
- J. M. Kahlenberg and M. J. Kaplan, “Little peptide, big effects: the role of LL-37 in inflammation and autoimmune disease,” J. Immunol. Baltim. Md 1950, vol. 191, no. 10, Nov. 2013.
D. S. Alexandre-Ramos et al., “LL-37 treatment on human peripheral blood mononuclear cells modulates immune response and promotes regulatory T-cells generation,” Biomed. Pharmacother. Biomedecine Pharmacother., vol. 108, pp. 1584–1590, Dec. 2018.
P. Y. Ong et al., “Endogenous antimicrobial peptides and skin infections in atopic dermatitis,” N. Engl. J. Med., vol. 347, no. 15, pp. 1151–1160, Oct. 2002.
C. D. Ciornei, T. Sigurdardóttir, A. Schmidtchen, and M. Bodelsson, “Antimicrobial and chemoattractant activity, lipopolysaccharide neutralization, cytotoxicity, and inhibition by serum of analogs of human cathelicidin LL-37,” Antimicrob. Agents Chemother., vol. 49, no. 7, pp. 2845–2850, Jul. 2005.
X. Chen et al., “Synergistic effect of antibacterial agents human β-defensins, cathelicidin LL-37 and lysozyme against Staphylococcus aureus and Escherichia coli,” J. Dermatol. Sci., vol. 40, no. 2, pp. 123–132, Nov. 2005.
M. Golec, “Cathelicidin LL-37: LPS-neutralizing, pleiotropic peptide,” Ann. Agric. Environ. Med. AAEM, vol. 14, no. 1, pp. 1–4, 2007.
R. Shaykhiev et al., “Human endogenous antibiotic LL-37 stimulates airway epithelial cell proliferation and wound closure,” Am. J. Physiol. Lung Cell. Mol. Physiol., vol. 789, no. 5, pp. L842-848, Nov. 2005.
M. H. Hoffmann et al., “The cathelicidins LL-37 and rCRAMP are associated with pathogenic events of arthritis in humans and rats,” Ann. Rheum. Dis., vol. 72, no. 7, pp. 1239–1248, Jul. 2013.
D. Kienhöfer et al., “No evidence of pathogenic involvement of cathelicidins in patient cohorts and mouse models of lupus and arthritis,” PloS One, vol. 9, no. 12, p. e115474, 2014.
L. N. Y. Chow et al., “Human cathelicidin LL-37-derived peptide IG-19 confers protection in a murine model of collagen-induced arthritis,” Mol. Immunol., vol. 57, no. 2, pp. 86–92, Feb. 2014.
K.-Y. G. Choi, S. Napper, and N. Mookherjee, “Human cathelicidin LL-37 and its derivative IG-19 regulate interleukin-32-induced inflammation,” Immunology, vol. 143, no. 1, pp. 68–80, Sep. 2014.
W. Zhu et al., “Arthritis is associated with T-cell-induced upregulation of Toll-like receptor 3 on synovial fibroblasts,” Arthritis Res. Ther., vol. 13, no. 3, p. R103, Jun. 2011.
K. L. Brown et al., “Host defense peptide LL-37 selectively reduces proinflammatory macrophage responses,” J. Immunol. Baltim. Md 1950, vol. 186, no. 9, pp. 5497–5505, May 2011.
J.-M. Otte et al., “Effects of the cathelicidin LL-37 on intestinal epithelial barrier integrity,” Regul. Pept., vol. 156, no. 1–3, pp. 104–117, Aug. 2009.
J.-M. Otte et al., “Human beta defensin 2 promotes intestinal wound healing in vitro,” J. Cell. Biochem., vol. 104, no. 6, pp. 2286–2297, Aug. 2008.
X. Chen et al., “Roles and Mechanisms of Human Cathelicidin LL-37 in Cancer,” Cell. Physiol. Biochem. Int. J. Exp. Cell. Physiol. Biochem. Pharmacol., vol. 47, no. 3, pp. 1060–1073, 2018.
Salvado M. Dolores, Di Gennaro Antonio, Lindbom Lennart, Agerberth Birgitta, and Haeggström Jesper Z., “Cathelicidin LL-37 Induces Angiogenesis via PGE2–EP3 Signaling in Endothelial Cells, In Vivo Inhibition by Aspirin,” Arterioscler. Thromb. Vasc. Biol., vol. 33, no. 8, pp. 1965–1972, Aug. 2013.
D. Xhindoli, S. Pacor, M. Benincasa, M. Scocchi, R. Gennaro, and A. Tossi, “The human cathelicidin LL-37 — A pore-forming antibacterial peptide and host-cell modulator,” Biochim. Biophys. Acta BBA – Biomembr., vol. 1858, no. 3, pp. 546–566, Mar. 2016.