Grátis (1) 30 ml de água bacteriostática
com ordens qualificadas sobreUS $ 500 USD.
(Exclui produtos de cápsula, peptídeos cosméticos, códigos promocionais e remessa)
O que é LL-37 (CAP-18)?
Estrutura LL-37

Pesquisa LL-37
LL-37 e doenças inflamatórias
O LL-37, apesar de anunciado principalmente como um peptídeo antimicrobiano, na verdade desempenha um papel em várias doenças inflamatórias, como psoríase, lúpus, artrite reumatóide e aterosclerose. Dependendo do ambiente inflamatório local e das células específicas envolvidas, o LL-37 possui vários comportamentos de modulação de sistema imunológico diferentes. Foi encontrado para:- decrease keratinocyte apoptosis,
- increase IFN-alpha production,
- alter chemotaxis of neutrophils and eosinophils,
- down-regulate signaling through toll-like receptor 4 (TLR4),
- aumentar a produção de IL-18 e
- diminuição dos níveis de placas ateroscleróticas[1].
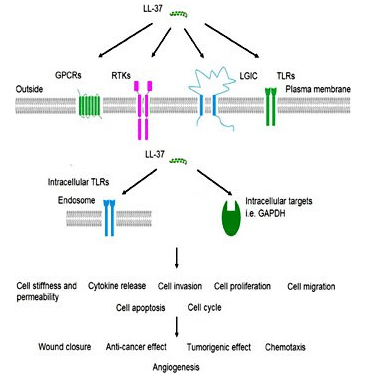
LL-37 é um antimicrobiano potente
O LL-37 faz parte do sistema imunológico inato e, como tal, é uma das primeiras peças do sistema imunológico a ser ativado durante a infecção. A pesquisa em infecções de pele sugere que a pele normal tem níveis muito baixos de LL-37, mas que o peptídeo se acumula rapidamente na presença de patógenos invasores. Foi demonstrado que o peptídeo funciona em conjunto com outras proteínas, como a beta-defensina humana 2 para combater a infecção[3]. LL-37 primarily works by binding to bacterial lipopolysaccharide (LPS), a major component of the outer membrane of gram-negative bacteria. LPS is a critical component of membrane integrity in these bacteria. The ability of LL-37 to bind to and interfere with LPS means it is exceptionally deadly to certain bacteria. There is interest in using the peptide exogenously to treat serious bacterial infections in people[4]. Despite the fact that LL-37 acts on the cell membrane components of gram-negative bacteria, it still has potent gram-positive effects as well. This could make it a beneficial treatment for staph infections and other serious bacteria. In vitro research indicates that LL-37 enhances the effects of lysozyme, an enzyme responsible for the destruction of gram positive bacteria like Staph aureus[5].LL-37 e doença pulmonar
O LPS, como mencionado acima, não é exclusivo das paredes celulares bacterianas. É encontrado em vários organismos diferentes e, em alguns casos, torna -se transportado pelo ar quando um ambiente é contaminado por mofo ou outros fungos. Quando o LPS é inalado, o tecido pulmonar normal responde produzindo. Infelizmente, a resposta geralmente é inadequada para impedir a síndrome da poeira tóxica e a patogênese de doenças respiratórias como asma, DPOC e muito mais. A pesquisa sobre o uso do LL-37 como um tratamento inalado para a síndrome do pó tóxico está em andamento[6]. One of the interesting findings of research into the effects of LL-37 on lung disease is that the peptide promotes epithelial cell proliferation and wound closure. It appears that one of the primary properties of LL-37, at least in the lungs, is to attract airway epithelial cells to the site of injury and promote both wound healing and the growth of blood vessels necessary for providing nutrients to the new tissue. It seems that LL-37 is an important homeostatic regulator in the airways just as it has been found to be a homeostatic regulator of immune function[7].Entendendo o LL-37 em artrite
A pesquisa em ratos indica que o LL-37 é encontrado em altas concentrações nas articulações afetadas pela artrite reumatóide. Em particular, o peptídeo parece estar associado aos eventos patológicos da artrite. Não está claro, no entanto, se o peptídeo for causador ou sua regulação positiva nessas articulações faz parte da tentativa do corpo de controlar o processo patológico[8]. Several things, however, suggest that LL-37 is beneficial in inflammation and not causative. First, there is no evidence that LL-37 or any other cathelicidin is involved in the pathogenesis of inflammatory disease. This does not rule the peptide out as being causative, the but evidence weighs pretty heavily against that being the case. In particular, LL-37 deficiency does not affect outcomes in animal models of arthritis or lupus. In other words, animals without LL-37 experience the same pathological progression as animals who have the peptide. Based on these findings, scientists have suggested that reactivity against cathelicidins in arthritis is likely an epiphenomenon that results from extensive over-expression of the peptide in inflamed tissues[9]. In other words, it is incidental. Research in mouse models of arthritis indicate that peptides derived from LL-37 confer protection against collagen damage that often occurs in inflammatory arthritis. Administration of these peptides directly to affected joints decreases the severity of disease as well as serum levels of antibody against type II collagens[10]. Com base neste estudo, é razoável especular que o LL-37 provavelmente tenha atividade protetora na artrite, o que poderia explicar suas altas concentrações nos tecidos com inflamação substancial. Esta especulação é apoiada pelo fato de que o LL-37 e seus derivados demonstraram regular a inflamação causada pela interleucina-32, uma molécula que foi diretamente associada à gravidade da artrite inflamatória[11]. Arthritis has also been associated with an up-regulation of toll-like receptor 3 in the fibroblasts of synovial fluid, a factor that likely aggravates arthritis by increasing inflammatory cytokine levels[12]. Foi demonstrado que o LL-37 se liga ao TLR4 e promove efeitos pró-inflamatórios ou anti-inflamatórios. O que faz no cenário da regulação positiva do TLR3 não é clara, mas a pesquisa está em andamento. A ideia de que pode reduzir a inflamação seletivamente não é irracional, pois foi encontrado que o LL-37 reduz seletivamente as respostas de macrófagos pró-inflamatórias no passado[13].LL-37 e o intestino
A pesquisa em culturas celulares indica que o LL-37 tem vários efeitos no intestino. Primeiro, o peptídeo aumenta a migração de células necessárias para manter a barreira epitelial do intestino. Segundo, o LL-37 reduz a apoptose no cenário de inflamação intestinal, ajudando a retardar a patogênese de várias condições inflamatórias. No geral, a pesquisa indica que o LL-37 pode ser um tratamento adjuvante útil em condições inflamatórias intestinais, após cirurgia intestinal ou no cenário de infecções intestinais agudas. Pode até ser útil como adjuvante da antibioticoterapia, ajudando a impedir os efeitos colaterais gastrointestinais que geralmente limitam o uso de antibióticos orais[14]. LL-37 does not work alone in the intestine, pairing once again with human beta defensin 2 to promote wound healing. Research in cell culture indicates that the peptides work in tandem to both repair and maintain intestinal epithelium while reducing TNF-related cell death[15]. Atualmente, os inibidores de TNF-alfa são um dos pilares do tratamento para condições inflamatórias intestinais. São medicamentos eficazes, mas têm vários efeitos colaterais graves, incluindo causar um aumento drástico no risco de infecção grave, como a tuberculose. O desenvolvimento de tratamentos baseados em LL-37 da doença inflamatória intestinal pode ajudar a reduzir a dependência dos inibidores de TNF-alfa e melhorar a morbimortalidade nessa população de pacientes.LL-37 e câncer intestinal
Pesquisas sobre LL-37 e câncer produziram resultados mistos, mas o peptídeo parece ser benéfico no cenário de câncer intestinal e gástrico, incluindo carcinoma espinocelular oral associado ao tabagismo e uso de tabaco. Curiosamente, esses efeitos parecem ser mediados por uma via dependente de vitamina-D, o que pode explicar por que tomar a vitamina foi anteriormente associado a um risco reduzido de câncer de IG. Parece que a vitamina D induz a atividade anticâncer dos macrófagos associados ao tumor via LL-37[16].LL-37 e crescimento dos vasos sanguíneos
O LL-37 parece desencadear a síntese da prostaglandina E2 (PGE2) nas células endoteliais. O PGE2 está associado à dor inflamatória e ao crescimento dos vasos sanguíneos, mas esses efeitos diferem com base em onde a molécula está sendo expressa. Nas células endoteliais, o PGE2 desencadeia o desenvolvimento de vasos sanguíneos em um processo chamado angiogênese[17]. Isso pode ser bom e ruim, dependendo da configuração específica. A capacidade de regular a angiogênese tem sido o foco de muitas pesquisas nas últimas décadas, porque afeta o desenvolvimento do câncer, doenças cardíacas, resultados de derrame, cicatrização de feridas e muito mais. A atividade de LL-37 oferece um meio útil para investigar a via da angiogênese, bem como um modelo para possíveis intervenções futuras para promover o crescimento dos vasos sanguíneos quando necessário (por exemplo, doença cardíaca) e desencorajá-la quando é prejudicial (por exemplo, câncer).Pesquisa em andamento LL-37
Autor do artigo
Autor da revista científica
Citações referenciadas
- J. M. Kahlenberg and M. J. Kaplan, “Little peptide, big effects: the role of LL-37 in inflammation and autoimmune disease,” J. Immunol. Baltim. Md 1950, vol. 191, no. 10, Nov. 2013.
D. S. Alexandre-Ramos et al., “LL-37 treatment on human peripheral blood mononuclear cells modulates immune response and promotes regulatory T-cells generation,” Biomed. Pharmacother. Biomedecine Pharmacother., vol. 108, pp. 1584–1590, Dec. 2018.
P. Y. Ong et al., “Endogenous antimicrobial peptides and skin infections in atopic dermatitis,” N. Engl. J. Med., vol. 347, no. 15, pp. 1151–1160, Oct. 2002.
C. D. Ciornei, T. Sigurdardóttir, A. Schmidtchen, and M. Bodelsson, “Antimicrobial and chemoattractant activity, lipopolysaccharide neutralization, cytotoxicity, and inhibition by serum of analogs of human cathelicidin LL-37,” Antimicrob. Agents Chemother., vol. 49, no. 7, pp. 2845–2850, Jul. 2005.
X. Chen et al., “Synergistic effect of antibacterial agents human β-defensins, cathelicidin LL-37 and lysozyme against Staphylococcus aureus and Escherichia coli,” J. Dermatol. Sci., vol. 40, no. 2, pp. 123–132, Nov. 2005.
M. Golec, “Cathelicidin LL-37: LPS-neutralizing, pleiotropic peptide,” Ann. Agric. Environ. Med. AAEM, vol. 14, no. 1, pp. 1–4, 2007.
R. Shaykhiev et al., “Human endogenous antibiotic LL-37 stimulates airway epithelial cell proliferation and wound closure,” Am. J. Physiol. Lung Cell. Mol. Physiol., vol. 789, no. 5, pp. L842-848, Nov. 2005.
M. H. Hoffmann et al., “The cathelicidins LL-37 and rCRAMP are associated with pathogenic events of arthritis in humans and rats,” Ann. Rheum. Dis., vol. 72, no. 7, pp. 1239–1248, Jul. 2013.
D. Kienhöfer et al., “No evidence of pathogenic involvement of cathelicidins in patient cohorts and mouse models of lupus and arthritis,” PloS One, vol. 9, no. 12, p. e115474, 2014.
L. N. Y. Chow et al., “Human cathelicidin LL-37-derived peptide IG-19 confers protection in a murine model of collagen-induced arthritis,” Mol. Immunol., vol. 57, no. 2, pp. 86–92, Feb. 2014.
K.-Y. G. Choi, S. Napper, and N. Mookherjee, “Human cathelicidin LL-37 and its derivative IG-19 regulate interleukin-32-induced inflammation,” Immunology, vol. 143, no. 1, pp. 68–80, Sep. 2014.
W. Zhu et al., “Arthritis is associated with T-cell-induced upregulation of Toll-like receptor 3 on synovial fibroblasts,” Arthritis Res. Ther., vol. 13, no. 3, p. R103, Jun. 2011.
K. L. Brown et al., “Host defense peptide LL-37 selectively reduces proinflammatory macrophage responses,” J. Immunol. Baltim. Md 1950, vol. 186, no. 9, pp. 5497–5505, May 2011.
J.-M. Otte et al., “Effects of the cathelicidin LL-37 on intestinal epithelial barrier integrity,” Regul. Pept., vol. 156, no. 1–3, pp. 104–117, Aug. 2009.
J.-M. Otte et al., “Human beta defensin 2 promotes intestinal wound healing in vitro,” J. Cell. Biochem., vol. 104, no. 6, pp. 2286–2297, Aug. 2008.
X. Chen et al., “Roles and Mechanisms of Human Cathelicidin LL-37 in Cancer,” Cell. Physiol. Biochem. Int. J. Exp. Cell. Physiol. Biochem. Pharmacol., vol. 47, no. 3, pp. 1060–1073, 2018.
Salvado M. Dolores, Di Gennaro Antonio, Lindbom Lennart, Agerberth Birgitta, and Haeggström Jesper Z., “Cathelicidin LL-37 Induces Angiogenesis via PGE2–EP3 Signaling in Endothelial Cells, In Vivo Inhibition by Aspirin,” Arterioscler. Thromb. Vasc. Biol., vol. 33, no. 8, pp. 1965–1972, Aug. 2013.
D. Xhindoli, S. Pacor, M. Benincasa, M. Scocchi, R. Gennaro, and A. Tossi, “The human cathelicidin LL-37 — A pore-forming antibacterial peptide and host-cell modulator,” Biochim. Biophys. Acta BBA – Biomembr., vol. 1858, no. 3, pp. 546–566, Mar. 2016.