ฟรี (1) น้ําแบคทีเรีย 30 มล.
เมื่อคําสั่งซื้อที่ผ่านการรับรองมากกว่า$ 500 เหรียญสหรัฐ.
(ไม่รวมผลิตภัณฑ์แคปซูล เปปไทด์เครื่องสําอาง รหัสโปรโมชั่น และการจัดส่ง)
ภาพรวม KEYWORDS-C
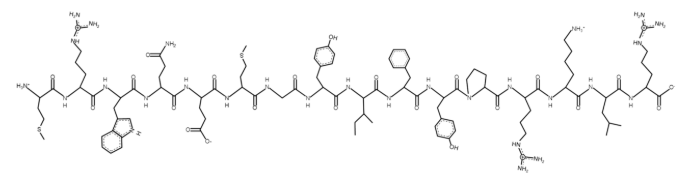
โครงสร้าง MOTS-c
การวิจัย MOTS-c
การเผาผลาญกล้ามเนื้อ
การวิจัยในหนูระบุว่า MOTS-c สามารถย้อนกลับการดื้อต่ออินซูลินที่ขึ้นกับอายุในกล้ามเนื้อ ซึ่งจะช่วยเพิ่มการดูดซึมกลูโคสของกล้ามเนื้อ ทําได้โดยการปรับปรุงการตอบสนองของกล้ามเนื้อโครงร่างต่อการกระตุ้น AMPK ซึ่งจะเพิ่มการแสดงออกของตัวขนส่งกลูโคส[1]. สิ่งสําคัญคือต้องสังเกตว่าการกระตุ้นนี้ไม่ขึ้นกับวิถีอินซูลิน ดังนั้นจึงเป็นทางเลือกอื่นในการเพิ่มการดูดซึมกลูโคสโดยกล้ามเนื้อเมื่ออินซูลินไม่ได้ผลหรือมีปริมาณไม่เพียงพอ ผลลัพธ์ที่ได้คือการทํางานของกล้ามเนื้อดีขึ้น การเจริญเติบโตของกล้ามเนื้อเพิ่มขึ้น และความต้านทานต่ออินซูลินที่ลดลงการเผาผลาญไขมัน
การวิจัยในหนูแสดงให้เห็นว่าระดับฮอร์โมนเอสโตรเจนต่ํานําไปสู่มวลไขมันที่เพิ่มขึ้นและความผิดปกติของเนื้อเยื่อไขมันปกติ สถานการณ์นี้เพิ่มความเสี่ยงในการเกิดการดื้อต่ออินซูลินและต่อมาความเสี่ยงในการเกิดโรคเบาหวาน อย่างไรก็ตาม การเสริมหนูด้วย MOTS-c จะช่วยเพิ่มการทํางานของไขมันสีน้ําตาลและลดการสะสมของเนื้อเยื่อไขมัน นอกจากนี้ยังปรากฏว่าเปปไทด์ป้องกันความผิดปกติของไขมันและการอักเสบของไขมันที่มักนําหน้าการดื้อต่ออินซูลิน[2]. It appears that at least part of the influence that MOTS-c has on fat metabolism is mediated through activation of the AMPK pathway. This well-defined pathway is turned on when cellular energy levels are low and it drives the uptake of both glucose and fatty acids by cells for metabolism. It is also the pathway that is activated in ketogenic diets, like the Atkin’s diet, which promote fat metabolism while protecting lean body mass. MOTS-c targets the methionine-folate cycle, increases AICAR levels, and activates AMPK. New research suggests that MOTS-c can actually leave the mitochondria and make its way to the nucleus where the peptide can affect nuclear gene expression. Following metabolic stress, MOTS-c has been shown to regulate nuclear genes involved in glucose restriction and antioxidant responses[3].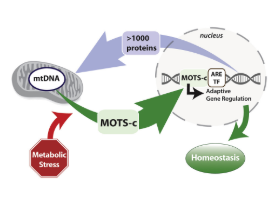
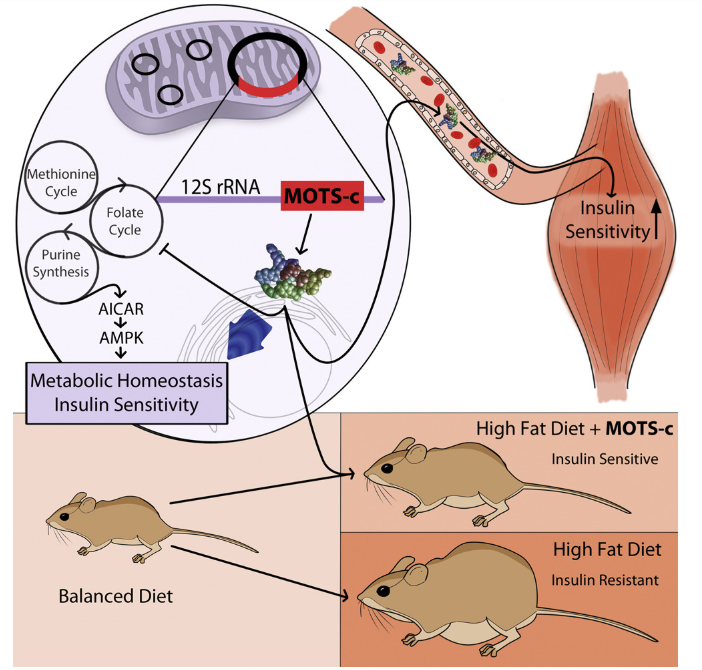
ความไวของอินซูลิน
การวิจัยที่วัดระดับ MOTS-c ในบุคคลที่ไวต่ออินซูลินและดื้อต่ออินซูลินแสดงให้เห็นว่าโปรตีนมีความเกี่ยวข้องกับความไวของอินซูลินเฉพาะในบุคคลที่ผอมเท่านั้น กล่าวอีกนัยหนึ่ง MOTS-c ดูเหมือนจะมีความสําคัญในการเกิดโรคของการไม่ไวต่ออินซูลิน แต่ไม่ใช่ในการรักษาสภาพ[6]. นักวิทยาศาสตร์คาดเดาว่าเปปไทด์อาจเป็นวิธีที่มีประโยชน์ในการตรวจสอบบุคคลที่ผอมแพ้ก่อนเป็นเบาหวาน และการเปลี่ยนแปลงของระดับ MOTS-c อาจทําหน้าที่เป็นสัญญาณเตือนล่วงหน้าของการไม่ไวต่ออินซูลินที่อาจเกิดขึ้น การเสริม MOTS-c ในการตั้งค่านี้สามารถช่วยยับยั้งการดื้อต่ออินซูลินและการพัฒนาของโรคเบาหวานได้ การวิจัยในหนูจนถึงตอนนี้มีแนวโน้มที่ดี แต่จําเป็นต้องทํางานเพิ่มเติมเพื่อทําความเข้าใจผลกระทบทั้งหมดของ MOTS-c ต่อการควบคุมอินซูลินโรคกระดูกพรุน
MOTS-c ดูเหมือนจะมีบทบาทในการสังเคราะห์คอลลาเจนชนิดที่ 1 โดยเซลล์กระดูกในกระดูก การวิจัยในสายเซลล์ osteoblast แสดงให้เห็นว่า MOTS-c ควบคุมวิถี TGF-beta/SMAD ที่รับผิดชอบต่อสุขภาพและการอยู่รอดของเซลล์กระดูก ด้วยการส่งเสริมการรอดชีวิตของเซลล์กระดูก MOTS-c ช่วยปรับปรุงการสังเคราะห์คอลลาเจนชนิดที่ 1 และด้วยเหตุนี้จึงทําให้ความแข็งแรงและความสมบูรณ์ของกระดูก[7]. Additional research in osteoporosis has revealed that MOTS-c promotes the differentiation of bone marrow stem cells via the same TGF-beta/SMAD pathway. In the study, this directly led to increased osteogenesis (formation of new bone)[8]. ดังนั้น MOTS-c ไม่เพียงแต่ปกป้อง osteoblasts และส่งเสริมการอยู่รอด แต่ยังส่งเสริมการพัฒนาจากสเต็มเซลล์อีกด้วยอายุยืน
การวิจัยเกี่ยวกับ MOTS-c ได้ระบุการเปลี่ยนแปลงเฉพาะของเปปไทด์ที่เกี่ยวข้องกับอายุยืนยาวในประชากรมนุษย์บางกลุ่ม เช่น ชาวญี่ปุ่น การเปลี่ยนแปลงของยีน MOTS-c ในกรณีนี้นําไปสู่การทดแทนสารตกค้างของกลูตาเมตสําหรับไลซีนที่ปกติจะพบในตําแหน่ง 14 ของโปรตีน ไม่ชัดเจนว่าการเปลี่ยนแปลงนี้ส่งผลต่อด้านการทํางานของโปรตีนอย่างไร แต่เกือบจะแน่นอนว่ากลูตาเมตมีคุณสมบัติที่แตกต่างจากไลซีนอย่างสิ้นเชิง และจะเปลี่ยนทั้งโครงสร้างและการทํางานของยีน MOTS-c จําเป็นต้องมีการวิจัยเพิ่มเติมเพื่อทําความเข้าใจว่าการเปลี่ยนแปลงนี้ส่งผลต่อการทํางานอย่างไร แต่พบเฉพาะในผู้ที่มีบรรพบุรุษในเอเชียตะวันออกเฉียงเหนือเท่านั้น และคิดว่ามีบทบาทในการมีอายุยืนยาวเป็นพิเศษที่เห็นในประชากรกลุ่มนี้[9]. According to Dr. Changhan David Lee, a researcher at the School of Gerontology at USC Leonard Davis, mitchondrial biology holds the keep to extending both lifespan and healthspan in humans. The mitochondria, being the single most important metabolic organelle, is “strongly implicated in aging and age-related diseases.” Until now, dietary restriction offered the only reliable means of affecting mitochondrial function and thus longevity. Peptides like MOTS-c, however, may make it possible to directly impact mitochondrial function in a more profound way.สุขภาพหัวใจ
การวิจัยที่วัดระดับ MOTS-c ในมนุษย์ที่ได้รับการตรวจหลอดเลือดหัวใจพบว่าผู้ป่วยที่มีระดับ MOTS-c ในเลือดต่ํากว่ามีระดับความผิดปกติของเซลล์เยื่อบุผนังหลอดเลือดสูงกว่า เซลล์เยื่อบุผนังหลอดเลือดเรียงรายอยู่ภายในหลอดเลือดและเป็นส่วนสําคัญในการควบคุมความดันโลหิตการแข็งตัวของเลือดและการก่อตัวของคราบจุลินทรีย์ การวิจัยเพิ่มเติมในหนูชี้ให้เห็นว่าแม้ว่า MOTS-c จะไม่ส่งผลโดยตรงต่อการตอบสนองของหลอดเลือด แต่ก็ทําให้เซลล์เยื่อบุผนังหลอดเลือดไวต่อผลกระทบของโมเลกุลส่งสัญญาณอื่นๆ เช่น อะซิทิลโคลีน การเสริม MOTS-c ในหนูช่วยปรับปรุงการทํางานของเยื่อบุผนังหลอดเลือดและปรับปรุงการทํางานของหลอดเลือดขนาดเล็กและเยื่อหุ้มหัวใจ[10]. MOTS-c is not alone among mitochondria-derived peptides (MDPs) in affecting heart health. Research suggests that at least three MDPs play roles in protecting cardiac cells against stress and inflammation. There is good reason to believe that MDP dysregulation is also an important factor in the development of cardiovascular disease. The peptides may even be important factors in reperfusion injury and, as pointed out above, in endothelial function[11]. MOTS-c exhibits minimal side effects, low oral and excellent subcutaneous bioavailability in mice. Per kg dosage in mice does not scale to humans. MOTS-c for sale atผู้เขียนบทความ
ผู้เขียนวารสารวิทยาศาสตร์

การอ้างอิงอ้างอิง
- C. Lee, K. H. Kim, and P. Cohen, “MOTS-c: A novel mitochondrial-derived peptide regulating muscle and fat metabolism,” Free Radic. Biol. Med., vol. 100, pp. 182–187, Nov. 2016. [PMC]
H. Lu et al., “MOTS-c peptide regulates adipose homeostasis to prevent ovariectomy-induced metabolic dysfunction,” J. Mol. Med. Berl. Ger., vol. 97, no. 4, pp. 473–485, Apr. 2019. [PubMed]
K. H. Kim, J. M. Son, B. A. Benayoun, and C. Lee, “The Mitochondrial-Encoded Peptide MOTS-c Translocates to the Nucleus to Regulate Nuclear Gene Expression in Response to Metabolic Stress,” Cell Metab., vol. 28, no. 3, pp. 516-524.e7, Sep. 2018. [PMC]
S.-J. Kim et al., “The mitochondrial-derived peptide MOTS-c is a regulator of plasma metabolites and enhances insulin sensitivity,” Physiol. Rep., vol. 7, no. 13, p. e14171, Jul. 2019. [PubMed]
R. Crescenzo, F. Bianco, A. Mazzoli, A. Giacco, G. Liverini, and S. Iossa, “A possible link between hepatic mitochondrial dysfunction and diet-induced insulin resistance,” Eur. J. Nutr., vol. 55, no. 1, pp. 1–6, Feb. 2016. [BMJ]
L. R. Cataldo, R. Fernández-Verdejo, J. L. Santos, and J. E. Galgani, “Plasma MOTS-c levels are associated with insulin sensitivity in lean but not in obese individuals,” J. Investig. Med., vol. 66, no. 6, pp. 1019–1022, Aug. 2018. [PubMed]
N. Che et al., “MOTS-c improves osteoporosis by promoting the synthesis of type I collagen in osteoblasts via TGF-β/SMAD signaling pathway,” Eur. Rev. Med. Pharmacol. Sci., vol. 23, no. 8, pp. 3183–3189, Apr. 2019. [PubMed]
B.-T. Hu and W.-Z. Chen, “MOTS-c improves osteoporosis by promoting osteogenic differentiation of bone marrow mesenchymal stem cells via TGF-β/Smad pathway,” Eur. Rev. Med. Pharmacol. Sci., vol. 22, no. 21, pp. 7156–7163, Nov. 2018. [PubMed]
N. Fuku et al., “The mitochondrial-derived peptide MOTS-c: A player in exceptional longevity?,” Aging Cell, vol. 14, Aug. 2015. [Research Gate]
Q. Qin et al., “Downregulation of circulating MOTS-c levels in patients with coronary endothelial dysfunction,” Int. J. Cardiol., vol. 254, pp. 23–27, 01 2018. [PubMed]
Y. Yang et al., “The role of mitochondria-derived peptides in cardiovascular disease: Recent updates,” Biomed. Pharmacother. Biomedecine Pharmacother., vol. 117, p. 109075, Jun. 2019. [PubMed]