MIỄN PHÍ (1) 30 ml nước vi khuẩn
với các đơn đặt hàng đủ điều kiện$ 500 USD.
(Không bao gồm các sản phẩm viên nang, peptide mỹ phẩm, mã khuyến mãi và vận chuyển)
LL-37 (CAP-18) là gì?
Cấu trúc LL-37

Nghiên cứu LL-37
LL-37 và các bệnh viêm
LL-37, trong khi chủ yếu được coi là một peptide kháng khuẩn, thực sự đóng vai trò trong một số bệnh viêm như bệnh vẩy nến, lupus, viêm khớp dạng thấp và xơ vữa động mạch. Tùy thuộc vào môi trường viêm cục bộ và các tế bào cụ thể liên quan, LL-37 có một số hành vi điều chế hệ thống miễn dịch khác nhau. Nó đã được tìm thấy:- decrease keratinocyte apoptosis,
- increase IFN-alpha production,
- alter chemotaxis of neutrophils and eosinophils,
- down-regulate signaling through toll-like receptor 4 (TLR4),
- tăng sản xuất IL-18 và
- Giảm mức độ xơ vữa động mạch[1].
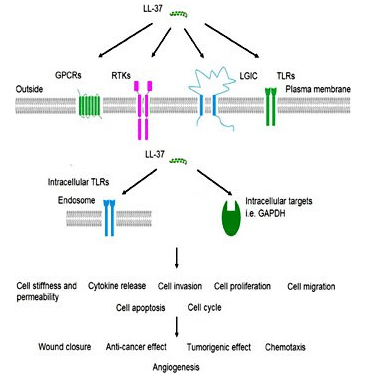
LL-37 là một loại thuốc kháng khuẩn mạnh
LL-37 là một phần của hệ thống miễn dịch bẩm sinh và như vậy là một trong những phần đầu tiên của hệ thống miễn dịch được kích hoạt trong quá trình nhiễm trùng. Nghiên cứu về nhiễm trùng da cho thấy rằng da bình thường có mức độ LL-37 rất thấp nhưng peptide tích tụ nhanh chóng với sự hiện diện của các mầm bệnh xâm nhập. Peptide đã được chứng minh là hoạt động song song với các protein khác, như beta-defensin 2 của con người để chống nhiễm trùng[3]. LL-37 primarily works by binding to bacterial lipopolysaccharide (LPS), a major component of the outer membrane of gram-negative bacteria. LPS is a critical component of membrane integrity in these bacteria. The ability of LL-37 to bind to and interfere with LPS means it is exceptionally deadly to certain bacteria. There is interest in using the peptide exogenously to treat serious bacterial infections in people[4]. Despite the fact that LL-37 acts on the cell membrane components of gram-negative bacteria, it still has potent gram-positive effects as well. This could make it a beneficial treatment for staph infections and other serious bacteria. In vitro research indicates that LL-37 enhances the effects of lysozyme, an enzyme responsible for the destruction of gram positive bacteria like Staph aureus[5].LL-37 và bệnh phổi
LPS, như đã đề cập ở trên, không phải là duy nhất đối với thành tế bào vi khuẩn. Nó được tìm thấy ở một số sinh vật khác nhau và, trong một số trường hợp, trở nên không khí khi môi trường bị nhiễm nấm mốc hoặc nấm khác. Khi LPS được hít vào, mô phổi bình thường phản ứng bằng cách sản xuất. Thật không may, phản ứng thường không đủ để ngăn ngừa hội chứng bụi độc hại và sinh bệnh học của các bệnh về đường hô hấp như hen suyễn, COPD, v.v. Nghiên cứu về việc sử dụng LL-37 như một phương pháp điều trị hít phải cho hội chứng bụi độc hại hiện đang được tiến hành[6]. One of the interesting findings of research into the effects of LL-37 on lung disease is that the peptide promotes epithelial cell proliferation and wound closure. It appears that one of the primary properties of LL-37, at least in the lungs, is to attract airway epithelial cells to the site of injury and promote both wound healing and the growth of blood vessels necessary for providing nutrients to the new tissue. It seems that LL-37 is an important homeostatic regulator in the airways just as it has been found to be a homeostatic regulator of immune function[7].Hiểu LL-37 trong viêm khớp
Nghiên cứu ở chuột chỉ ra rằng LL-37 được tìm thấy ở nồng độ cao trong các khớp bị ảnh hưởng bởi viêm khớp dạng thấp. Đặc biệt, peptide dường như có liên quan đến các sự kiện bệnh lý của viêm khớp. Tuy nhiên, rõ ràng là nếu peptide là nguyên nhân hoặc điều chỉnh tăng của nó trong các khớp này là một phần của cơ thể cố gắng kiểm soát quá trình bệnh lý[8]. Several things, however, suggest that LL-37 is beneficial in inflammation and not causative. First, there is no evidence that LL-37 or any other cathelicidin is involved in the pathogenesis of inflammatory disease. This does not rule the peptide out as being causative, the but evidence weighs pretty heavily against that being the case. In particular, LL-37 deficiency does not affect outcomes in animal models of arthritis or lupus. In other words, animals without LL-37 experience the same pathological progression as animals who have the peptide. Based on these findings, scientists have suggested that reactivity against cathelicidins in arthritis is likely an epiphenomenon that results from extensive over-expression of the peptide in inflamed tissues[9]. In other words, it is incidental. Research in mouse models of arthritis indicate that peptides derived from LL-37 confer protection against collagen damage that often occurs in inflammatory arthritis. Administration of these peptides directly to affected joints decreases the severity of disease as well as serum levels of antibody against type II collagens[10]. Dựa trên nghiên cứu này, thật hợp lý khi suy đoán rằng LL-37 có thể có hoạt động bảo vệ trong viêm khớp, điều này có thể giải thích nồng độ cao của nó trong các mô với viêm đáng kể. Sự suy đoán này được hỗ trợ bởi thực tế là LL-37 và các dẫn xuất của nó đã được chứng minh là điều chỉnh viêm do interleukin-32, một phân tử có liên quan trực tiếp đến mức độ nghiêm trọng của viêm khớp viêm viêm[11]. Arthritis has also been associated with an up-regulation of toll-like receptor 3 in the fibroblasts of synovial fluid, a factor that likely aggravates arthritis by increasing inflammatory cytokine levels[12]. LL-37 đã được chứng minh là liên kết với TLR4 và thúc đẩy các tác dụng gây viêm hoặc chống viêm. Điều đó trong môi trường điều chỉnh tăng TLR3 không rõ ràng, nhưng nghiên cứu đang diễn ra. Ý tưởng rằng nó có thể làm giảm viêm một cách có chọn lọc là không hợp lý khi LL-37 đã được tìm thấy để giảm chọn lọc các phản ứng đại thực bào gây viêm trong quá khứ[13].LL-37 và ruột
Nghiên cứu trong nuôi cấy tế bào chỉ ra rằng LL-37 có một số ảnh hưởng trong ruột. Đầu tiên, peptide làm tăng sự di chuyển của các tế bào cần thiết để duy trì hàng rào biểu mô của ruột. Thứ hai, LL-37 làm giảm apoptosis trong môi trường viêm ruột, giúp làm chậm sinh bệnh học của một số tình trạng viêm. Nhìn chung, nghiên cứu chỉ ra rằng LL-37 có thể là một phương pháp điều trị bổ trợ hữu ích trong tình trạng ruột viêm, sau phẫu thuật đường ruột hoặc trong bối cảnh nhiễm trùng đường ruột cấp tính. Nó thậm chí có thể chứng minh hữu ích như một chất bổ trợ cho liệu pháp kháng sinh, giúp ngăn ngừa các tác dụng phụ của GI thường hạn chế sử dụng kháng sinh đường uống[14]. LL-37 does not work alone in the intestine, pairing once again with human beta defensin 2 to promote wound healing. Research in cell culture indicates that the peptides work in tandem to both repair and maintain intestinal epithelium while reducing TNF-related cell death[15]. Hiện tại, các chất ức chế TNF-alpha là một phương pháp điều trị chính cho tình trạng viêm ruột. Chúng là các loại thuốc hiệu quả, nhưng có một số tác dụng phụ nghiêm trọng bao gồm gây ra sự gia tăng mạnh mẽ nguy cơ nhiễm trùng nghiêm trọng, chẳng hạn như bệnh lao. Sự phát triển của các phương pháp điều trị bệnh viêm ruột dựa trên LL-37 có thể giúp giảm sự phụ thuộc vào các chất ức chế TNF-alpha và cải thiện tỷ lệ mắc bệnh và tử vong trong dân số bệnh nhân này.LL-37 và ung thư đường ruột
Nghiên cứu về LL-37 và ung thư đã tạo ra kết quả hỗn hợp, nhưng peptide dường như có lợi trong việc ung thư ruột và dạ dày, bao gồm ung thư biểu mô tế bào vảy miệng liên quan đến việc sử dụng hút thuốc và thuốc lá. Thật thú vị, những tác dụng này dường như được trung gian bởi con đường phụ thuộc vitamin-D, điều này có thể giải thích tại sao dùng vitamin trước đây có liên quan đến giảm nguy cơ ung thư GI. Dường như vitamin D gây ra hoạt động chống ung thư của các đại thực bào liên quan đến khối u thông qua LL-37[16].LL-37 và tăng trưởng mạch máu
LL-37 dường như kích hoạt sự tổng hợp của prostaglandin E2 (PGE2) trong các tế bào nội mô. PGE2 có liên quan đến cả đau viêm và với sự phát triển của các mạch máu, nhưng những hiệu ứng này khác nhau dựa trên nơi phân tử đang được thể hiện. Trong các tế bào nội mô, PGE2 kích hoạt sự phát triển của các mạch máu trong một quá trình gọi là hình thành mạch[17]. Điều này có thể cả tốt và xấu, tùy thuộc vào cài đặt cụ thể. Khả năng điều chỉnh sự hình thành mạch là trọng tâm của nhiều nghiên cứu trong nhiều thập kỷ qua vì nó ảnh hưởng đến sự phát triển ung thư, bệnh tim, kết quả đột quỵ, chữa lành vết thương, v.v. Hoạt động LL-37 cung cấp một phương tiện hữu ích để thăm dò con đường tạo mạch cũng như mô hình cho các can thiệp tiềm năng trong tương lai để thúc đẩy sự phát triển của mạch máu khi cần thiết (ví dụ: bệnh tim) và không khuyến khích nó khi nó gây hại (ví dụ: ung thư).Nghiên cứu liên tục LL-37
Tác giả bài báo
Tạp chí khoa học tác giả
Trích dẫn được tham chiếu
- J. M. Kahlenberg and M. J. Kaplan, “Little peptide, big effects: the role of LL-37 in inflammation and autoimmune disease,” J. Immunol. Baltim. Md 1950, vol. 191, no. 10, Nov. 2013.
D. S. Alexandre-Ramos et al., “LL-37 treatment on human peripheral blood mononuclear cells modulates immune response and promotes regulatory T-cells generation,” Biomed. Pharmacother. Biomedecine Pharmacother., vol. 108, pp. 1584–1590, Dec. 2018.
P. Y. Ong et al., “Endogenous antimicrobial peptides and skin infections in atopic dermatitis,” N. Engl. J. Med., vol. 347, no. 15, pp. 1151–1160, Oct. 2002.
C. D. Ciornei, T. Sigurdardóttir, A. Schmidtchen, and M. Bodelsson, “Antimicrobial and chemoattractant activity, lipopolysaccharide neutralization, cytotoxicity, and inhibition by serum of analogs of human cathelicidin LL-37,” Antimicrob. Agents Chemother., vol. 49, no. 7, pp. 2845–2850, Jul. 2005.
X. Chen et al., “Synergistic effect of antibacterial agents human β-defensins, cathelicidin LL-37 and lysozyme against Staphylococcus aureus and Escherichia coli,” J. Dermatol. Sci., vol. 40, no. 2, pp. 123–132, Nov. 2005.
M. Golec, “Cathelicidin LL-37: LPS-neutralizing, pleiotropic peptide,” Ann. Agric. Environ. Med. AAEM, vol. 14, no. 1, pp. 1–4, 2007.
R. Shaykhiev et al., “Human endogenous antibiotic LL-37 stimulates airway epithelial cell proliferation and wound closure,” Am. J. Physiol. Lung Cell. Mol. Physiol., vol. 789, no. 5, pp. L842-848, Nov. 2005.
M. H. Hoffmann et al., “The cathelicidins LL-37 and rCRAMP are associated with pathogenic events of arthritis in humans and rats,” Ann. Rheum. Dis., vol. 72, no. 7, pp. 1239–1248, Jul. 2013.
D. Kienhöfer et al., “No evidence of pathogenic involvement of cathelicidins in patient cohorts and mouse models of lupus and arthritis,” PloS One, vol. 9, no. 12, p. e115474, 2014.
L. N. Y. Chow et al., “Human cathelicidin LL-37-derived peptide IG-19 confers protection in a murine model of collagen-induced arthritis,” Mol. Immunol., vol. 57, no. 2, pp. 86–92, Feb. 2014.
K.-Y. G. Choi, S. Napper, and N. Mookherjee, “Human cathelicidin LL-37 and its derivative IG-19 regulate interleukin-32-induced inflammation,” Immunology, vol. 143, no. 1, pp. 68–80, Sep. 2014.
W. Zhu et al., “Arthritis is associated with T-cell-induced upregulation of Toll-like receptor 3 on synovial fibroblasts,” Arthritis Res. Ther., vol. 13, no. 3, p. R103, Jun. 2011.
K. L. Brown et al., “Host defense peptide LL-37 selectively reduces proinflammatory macrophage responses,” J. Immunol. Baltim. Md 1950, vol. 186, no. 9, pp. 5497–5505, May 2011.
J.-M. Otte et al., “Effects of the cathelicidin LL-37 on intestinal epithelial barrier integrity,” Regul. Pept., vol. 156, no. 1–3, pp. 104–117, Aug. 2009.
J.-M. Otte et al., “Human beta defensin 2 promotes intestinal wound healing in vitro,” J. Cell. Biochem., vol. 104, no. 6, pp. 2286–2297, Aug. 2008.
X. Chen et al., “Roles and Mechanisms of Human Cathelicidin LL-37 in Cancer,” Cell. Physiol. Biochem. Int. J. Exp. Cell. Physiol. Biochem. Pharmacol., vol. 47, no. 3, pp. 1060–1073, 2018.
Salvado M. Dolores, Di Gennaro Antonio, Lindbom Lennart, Agerberth Birgitta, and Haeggström Jesper Z., “Cathelicidin LL-37 Induces Angiogenesis via PGE2–EP3 Signaling in Endothelial Cells, In Vivo Inhibition by Aspirin,” Arterioscler. Thromb. Vasc. Biol., vol. 33, no. 8, pp. 1965–1972, Aug. 2013.
D. Xhindoli, S. Pacor, M. Benincasa, M. Scocchi, R. Gennaro, and A. Tossi, “The human cathelicidin LL-37 — A pore-forming antibacterial peptide and host-cell modulator,” Biochim. Biophys. Acta BBA – Biomembr., vol. 1858, no. 3, pp. 546–566, Mar. 2016.