Bebas (1) 30 mL air bakteriostatik
dengan pesanan yang memenuhi syarat$ 500 USD.
(Tidak termasuk produk kapsul, peptida kosmetik, kode promo dan pengiriman)
Apa itu LL-37 (CAP-18)?
Struktur LL-37

Penelitian LL-37
LL-37 dan penyakit radang
LL-37, sementara terutama disebut sebagai peptida antimikroba, sebenarnya berperan dalam sejumlah penyakit radang seperti psoriasis, lupus, rheumatoid arthritis, dan aterosklerosis. Bergantung pada lingkungan peradangan lokal dan sel-sel tertentu yang terlibat, LL-37 memiliki beberapa perilaku modulasi sistem kekebalan tubuh yang berbeda. Itu telah ditemukan untuk:- decrease keratinocyte apoptosis,
- increase IFN-alpha production,
- alter chemotaxis of neutrophils and eosinophils,
- down-regulate signaling through toll-like receptor 4 (TLR4),
- meningkatkan produksi IL-18, dan
- Penurunan kadar plak aterosklerotik[1].
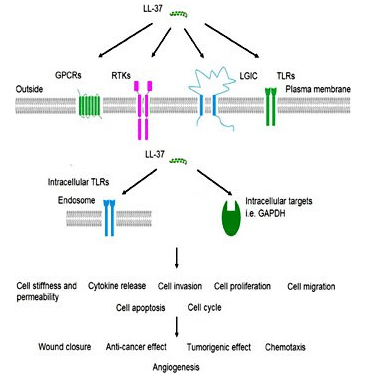
LL-37 adalah antimikroba yang kuat
LL-37 adalah bagian dari sistem kekebalan tubuh bawaan dan dengan demikian adalah salah satu bagian pertama dari sistem kekebalan yang diaktifkan selama infeksi. Penelitian dalam infeksi kulit menunjukkan bahwa kulit normal memiliki kadar LL-37 yang sangat rendah tetapi peptida terakumulasi dengan cepat di hadapan patogen yang menyerang. Peptida telah terbukti bekerja seiring dengan protein lain, seperti beta-defensin 2 untuk memerangi infeksi[3]. LL-37 primarily works by binding to bacterial lipopolysaccharide (LPS), a major component of the outer membrane of gram-negative bacteria. LPS is a critical component of membrane integrity in these bacteria. The ability of LL-37 to bind to and interfere with LPS means it is exceptionally deadly to certain bacteria. There is interest in using the peptide exogenously to treat serious bacterial infections in people[4]. Despite the fact that LL-37 acts on the cell membrane components of gram-negative bacteria, it still has potent gram-positive effects as well. This could make it a beneficial treatment for staph infections and other serious bacteria. In vitro research indicates that LL-37 enhances the effects of lysozyme, an enzyme responsible for the destruction of gram positive bacteria like Staph aureus[5].Penyakit LL-37 dan paru-paru
LPS, seperti yang disebutkan di atas, tidak unik untuk dinding sel bakteri. Ini ditemukan dalam sejumlah organisme yang berbeda dan, dalam beberapa kasus, menjadi udara ketika lingkungan terkontaminasi oleh jamur atau jamur lainnya. Ketika LPS dihirup, jaringan paru -paru normal merespons dengan memproduksi. Sayangnya, responsnya sering tidak memadai untuk mencegah sindrom debu beracun dan patogenesis penyakit pernapasan seperti asma, COPD, dan banyak lagi. Penelitian tentang penggunaan LL-37 sebagai pengobatan inhalasi untuk sindrom debu beracun saat ini sedang berlangsung[6]. One of the interesting findings of research into the effects of LL-37 on lung disease is that the peptide promotes epithelial cell proliferation and wound closure. It appears that one of the primary properties of LL-37, at least in the lungs, is to attract airway epithelial cells to the site of injury and promote both wound healing and the growth of blood vessels necessary for providing nutrients to the new tissue. It seems that LL-37 is an important homeostatic regulator in the airways just as it has been found to be a homeostatic regulator of immune function[7].Memahami LL-37 dalam Arthritis
Penelitian pada tikus menunjukkan bahwa LL-37 ditemukan dalam konsentrasi tinggi pada sendi yang dipengaruhi oleh rheumatoid arthritis. Secara khusus, peptida tampaknya terkait dengan peristiwa patologis artritis. Namun, tidak jelas jika peptida itu sebab-akibat atau regulasi yang lebih tinggi pada sendi ini adalah bagian dari upaya tubuh untuk mengendalikan proses patologis[8]. Several things, however, suggest that LL-37 is beneficial in inflammation and not causative. First, there is no evidence that LL-37 or any other cathelicidin is involved in the pathogenesis of inflammatory disease. This does not rule the peptide out as being causative, the but evidence weighs pretty heavily against that being the case. In particular, LL-37 deficiency does not affect outcomes in animal models of arthritis or lupus. In other words, animals without LL-37 experience the same pathological progression as animals who have the peptide. Based on these findings, scientists have suggested that reactivity against cathelicidins in arthritis is likely an epiphenomenon that results from extensive over-expression of the peptide in inflamed tissues[9]. In other words, it is incidental. Research in mouse models of arthritis indicate that peptides derived from LL-37 confer protection against collagen damage that often occurs in inflammatory arthritis. Administration of these peptides directly to affected joints decreases the severity of disease as well as serum levels of antibody against type II collagens[10]. Berdasarkan penelitian ini, masuk akal untuk berspekulasi bahwa LL-37 mungkin memiliki aktivitas protektif dalam radang sendi, yang dapat menjelaskan konsentrasi jaringan yang tinggi dengan peradangan yang substansial. Spekulasi ini didukung oleh fakta bahwa LL-37 dan turunannya telah terbukti mengatur peradangan yang disebabkan oleh interleukin-32, molekul yang telah secara langsung terkait dengan keparahan radang sendi radang[11]. Arthritis has also been associated with an up-regulation of toll-like receptor 3 in the fibroblasts of synovial fluid, a factor that likely aggravates arthritis by increasing inflammatory cytokine levels[12]. LL-37 telah terbukti mengikat TLR4 dan baik mempromosikan efek proinflamasi atau anti-inflamasi. Yang dilakukannya dalam pengaturan up-regulasi TLR3 tidak jelas, tetapi penelitian sedang berlangsung. Gagasan bahwa itu mungkin mengurangi peradangan secara selektif tidak masuk akal mengingat LL-37 telah ditemukan secara selektif mengurangi respons makrofag pro-inflamasi di masa lalu[13].LL-37 dan usus
Penelitian dalam kultur sel menunjukkan bahwa LL-37 memiliki beberapa efek di usus. Pertama, peptida meningkatkan migrasi sel yang diperlukan untuk mempertahankan penghalang epitel usus. Kedua, LL-37 mengurangi apoptosis dalam pengaturan peradangan usus, membantu memperlambat patogenesis sejumlah kondisi peradangan. Secara keseluruhan, penelitian menunjukkan bahwa LL-37 mungkin merupakan pengobatan ajuvan yang berguna dalam kondisi usus inflamasi, setelah operasi usus, atau dalam pengaturan infeksi usus akut. Bahkan mungkin terbukti bermanfaat sebagai adjuvan untuk terapi antibiotik, membantu mencegah efek samping GI yang sering membatasi penggunaan antibiotik oral[14]. LL-37 does not work alone in the intestine, pairing once again with human beta defensin 2 to promote wound healing. Research in cell culture indicates that the peptides work in tandem to both repair and maintain intestinal epithelium while reducing TNF-related cell death[15]. Saat ini, inhibitor TNF-alpha adalah pengobatan utama untuk kondisi radang usus. Mereka adalah obat yang efektif, tetapi memiliki sejumlah efek samping yang serius termasuk menyebabkan peningkatan risiko infeksi serius secara drastis, seperti tuberkulosis. Perkembangan perawatan berbasis LL-37 dari penyakit radang usus dapat membantu mengurangi ketergantungan pada inhibitor TNF-alpha dan meningkatkan morbiditas dan mortalitas pada populasi pasien ini.LL-37 dan kanker usus
Penelitian mengenai LL-37 dan kanker telah menghasilkan hasil yang beragam, tetapi peptida tampaknya bermanfaat dalam pengaturan kanker usus dan lambung, termasuk karsinoma sel skuamosa oral yang terkait dengan merokok dan penggunaan tembakau. Menariknya, efek ini tampaknya dimediasi oleh jalur yang bergantung pada vitamin, yang dapat menjelaskan mengapa menggunakan vitamin sebelumnya telah dikaitkan dengan pengurangan risiko kanker GI. Tampaknya vitamin D menginduksi aktivitas anti-kanker makrofag terkait tumor melalui LL-37[16].LL-37 dan pertumbuhan pembuluh darah
LL-37 tampaknya memicu sintesis prostaglandin E2 (PGE2) dalam sel endotel. PGE2 dikaitkan dengan nyeri inflamasi dan dengan pertumbuhan pembuluh darah, tetapi efek ini berbeda berdasarkan di mana molekul diekspresikan. Dalam sel endotel, PGE2 memicu perkembangan pembuluh darah dalam proses yang disebut angiogenesis[17]. Ini bisa baik dan buruk, tergantung pada pengaturan tertentu. Kemampuan untuk mengatur angiogenesis telah menjadi fokus banyak penelitian dalam beberapa dekade terakhir karena berdampak pada perkembangan kanker, penyakit jantung, hasil stroke, penyembuhan luka, dan banyak lagi. Aktivitas LL-37 menawarkan cara yang berguna untuk menyelidiki jalur angiogenesis serta model untuk intervensi potensial di masa depan untuk mempromosikan pertumbuhan pembuluh darah saat dibutuhkan (mis. Penyakit jantung) dan mencegahnya ketika merugikan (mis. Kanker).Penelitian LL-37 yang sedang berlangsung
Penulis artikel
Penulis Jurnal Ilmiah
Kutipan yang direferensikan
- J. M. Kahlenberg and M. J. Kaplan, “Little peptide, big effects: the role of LL-37 in inflammation and autoimmune disease,” J. Immunol. Baltim. Md 1950, vol. 191, no. 10, Nov. 2013.
D. S. Alexandre-Ramos et al., “LL-37 treatment on human peripheral blood mononuclear cells modulates immune response and promotes regulatory T-cells generation,” Biomed. Pharmacother. Biomedecine Pharmacother., vol. 108, pp. 1584–1590, Dec. 2018.
P. Y. Ong et al., “Endogenous antimicrobial peptides and skin infections in atopic dermatitis,” N. Engl. J. Med., vol. 347, no. 15, pp. 1151–1160, Oct. 2002.
C. D. Ciornei, T. Sigurdardóttir, A. Schmidtchen, and M. Bodelsson, “Antimicrobial and chemoattractant activity, lipopolysaccharide neutralization, cytotoxicity, and inhibition by serum of analogs of human cathelicidin LL-37,” Antimicrob. Agents Chemother., vol. 49, no. 7, pp. 2845–2850, Jul. 2005.
X. Chen et al., “Synergistic effect of antibacterial agents human β-defensins, cathelicidin LL-37 and lysozyme against Staphylococcus aureus and Escherichia coli,” J. Dermatol. Sci., vol. 40, no. 2, pp. 123–132, Nov. 2005.
M. Golec, “Cathelicidin LL-37: LPS-neutralizing, pleiotropic peptide,” Ann. Agric. Environ. Med. AAEM, vol. 14, no. 1, pp. 1–4, 2007.
R. Shaykhiev et al., “Human endogenous antibiotic LL-37 stimulates airway epithelial cell proliferation and wound closure,” Am. J. Physiol. Lung Cell. Mol. Physiol., vol. 789, no. 5, pp. L842-848, Nov. 2005.
M. H. Hoffmann et al., “The cathelicidins LL-37 and rCRAMP are associated with pathogenic events of arthritis in humans and rats,” Ann. Rheum. Dis., vol. 72, no. 7, pp. 1239–1248, Jul. 2013.
D. Kienhöfer et al., “No evidence of pathogenic involvement of cathelicidins in patient cohorts and mouse models of lupus and arthritis,” PloS One, vol. 9, no. 12, p. e115474, 2014.
L. N. Y. Chow et al., “Human cathelicidin LL-37-derived peptide IG-19 confers protection in a murine model of collagen-induced arthritis,” Mol. Immunol., vol. 57, no. 2, pp. 86–92, Feb. 2014.
K.-Y. G. Choi, S. Napper, and N. Mookherjee, “Human cathelicidin LL-37 and its derivative IG-19 regulate interleukin-32-induced inflammation,” Immunology, vol. 143, no. 1, pp. 68–80, Sep. 2014.
W. Zhu et al., “Arthritis is associated with T-cell-induced upregulation of Toll-like receptor 3 on synovial fibroblasts,” Arthritis Res. Ther., vol. 13, no. 3, p. R103, Jun. 2011.
K. L. Brown et al., “Host defense peptide LL-37 selectively reduces proinflammatory macrophage responses,” J. Immunol. Baltim. Md 1950, vol. 186, no. 9, pp. 5497–5505, May 2011.
J.-M. Otte et al., “Effects of the cathelicidin LL-37 on intestinal epithelial barrier integrity,” Regul. Pept., vol. 156, no. 1–3, pp. 104–117, Aug. 2009.
J.-M. Otte et al., “Human beta defensin 2 promotes intestinal wound healing in vitro,” J. Cell. Biochem., vol. 104, no. 6, pp. 2286–2297, Aug. 2008.
X. Chen et al., “Roles and Mechanisms of Human Cathelicidin LL-37 in Cancer,” Cell. Physiol. Biochem. Int. J. Exp. Cell. Physiol. Biochem. Pharmacol., vol. 47, no. 3, pp. 1060–1073, 2018.
Salvado M. Dolores, Di Gennaro Antonio, Lindbom Lennart, Agerberth Birgitta, and Haeggström Jesper Z., “Cathelicidin LL-37 Induces Angiogenesis via PGE2–EP3 Signaling in Endothelial Cells, In Vivo Inhibition by Aspirin,” Arterioscler. Thromb. Vasc. Biol., vol. 33, no. 8, pp. 1965–1972, Aug. 2013.
D. Xhindoli, S. Pacor, M. Benincasa, M. Scocchi, R. Gennaro, and A. Tossi, “The human cathelicidin LL-37 — A pore-forming antibacterial peptide and host-cell modulator,” Biochim. Biophys. Acta BBA – Biomembr., vol. 1858, no. 3, pp. 546–566, Mar. 2016.