遊離(1)30 mlの細菌性水
資格のある注文があります500米ドル.
(カプセル製品、化粧品ペプチド、プロモーションコード、出荷を除く)
LL-37は、すべてのカテリシジンと同様に、抗菌性、抗菌性、抗ウイルス性、抗真菌性を有しており、炎症を軽減することが示されています。また、研究では、特定の癌に対するその効果が示されており、特定の設定での血管の成長を促進しています。
製品の使用:この製品は、研究化学物質としてのみ意図されています。この指定により、in vitroテストと実験室の実験のために、研究化学物質を厳密に使用することができます。このウェブサイトで利用可能なすべての製品情報は、教育目的のみを目的としています。あらゆる種類の人間や動物への身体導入は、法律によって厳密に禁じられています。この製品は、認可された資格のある専門家によってのみ処理される必要があります。この製品は薬物、食品、または化粧品ではなく、薬物、食品、化粧品として誤ってブランド化されたり、誤用されたり、誤ったりしたりすることはない場合があります。
LL-37(CAP-18)とは何ですか?
LL-37は、多様な機能を持つ大型タンパク質ファミリーである唯一の既知のヒトカテリシジンです。これらのペプチドは、主にマクロファージと多核白血球(両方のタイプの白血球)に見られ、細菌を殺すために重要ですが、他の劇的な効果もあることがわかっています。クラス全体は、多くの場合、抗菌ペプチド(AMP)と呼ばれます。 LL-37は、自己免疫疾患、癌、創傷治癒において重要な役割を果たすことがわかっています。
LL-37構造

LL-37研究
LL-37および炎症性疾患
LL-37は、主に抗菌性ペプチドとして請求されていますが、実際には乾癬、ループス、関節リウマチ、アテローム性動脈硬化症などの多くの炎症性疾患に役割を果たしています。局所的な炎症環境と関係する特定の細胞に応じて、LL-37にはいくつかの異なる免疫系が挙動を調節しています。それは次のことがわかっています:- decrease keratinocyte apoptosis,
- increase IFN-alpha production,
- alter chemotaxis of neutrophils and eosinophils,
- down-regulate signaling through toll-like receptor 4 (TLR4),
- IL-18生産を増やします
- アテローム性動脈硬化性プラークのレベルを低下させます[1].
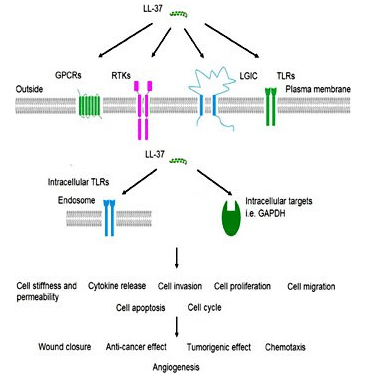
LL-37は強力な抗菌薬です
LL-37は自然免疫系の一部であり、感染中に活性化される免疫系の最初の部分の1つです。皮膚感染症の研究は、正常な皮膚のLL-37のレベルが非常に低いが、侵入病原体の存在下でペプチドが急速に蓄積することを示唆しています。ペプチドは、感染と戦うためにヒトベータ - ディフェンシン2のような他のタンパク質と連携して機能することが示されています[3]. LL-37 primarily works by binding to bacterial lipopolysaccharide (LPS), a major component of the outer membrane of gram-negative bacteria. LPS is a critical component of membrane integrity in these bacteria. The ability of LL-37 to bind to and interfere with LPS means it is exceptionally deadly to certain bacteria. There is interest in using the peptide exogenously to treat serious bacterial infections in people[4]. Despite the fact that LL-37 acts on the cell membrane components of gram-negative bacteria, it still has potent gram-positive effects as well. This could make it a beneficial treatment for staph infections and other serious bacteria. In vitro research indicates that LL-37 enhances the effects of lysozyme, an enzyme responsible for the destruction of gram positive bacteria like Staph aureus[5].LL-37および肺疾患
上記のように、LPSは細菌細胞壁に固有のものではありません。それは多くの異なる生物で見られ、場合によっては、環境がカビや他の菌類によって汚染されているときに空中になります。 LPSが吸入されると、生成することにより正常な肺組織が反応します。残念ながら、毒性粉塵症候群と喘息、COPDなどの呼吸器疾患の病因を予防するには、反応が不十分です。毒性粉塵症候群の吸入治療としてのLL-37の使用に関する研究が現在進行中です[6]. One of the interesting findings of research into the effects of LL-37 on lung disease is that the peptide promotes epithelial cell proliferation and wound closure. It appears that one of the primary properties of LL-37, at least in the lungs, is to attract airway epithelial cells to the site of injury and promote both wound healing and the growth of blood vessels necessary for providing nutrients to the new tissue. It seems that LL-37 is an important homeostatic regulator in the airways just as it has been found to be a homeostatic regulator of immune function[7].関節炎におけるLL-37の理解
ラットの研究は、LL-37が関節リウマチの影響を受けた関節の高濃度で見られることを示しています。特に、ペプチドは関節炎の病理学的事象に関連しているようです。ただし、ペプチドが原因であるか、これらの関節におけるそのアップレギュレーションが病理学的プロセスを制御しようとする体の試みの一部である場合、それは明確ではありません[8]. Several things, however, suggest that LL-37 is beneficial in inflammation and not causative. First, there is no evidence that LL-37 or any other cathelicidin is involved in the pathogenesis of inflammatory disease. This does not rule the peptide out as being causative, the but evidence weighs pretty heavily against that being the case. In particular, LL-37 deficiency does not affect outcomes in animal models of arthritis or lupus. In other words, animals without LL-37 experience the same pathological progression as animals who have the peptide. Based on these findings, scientists have suggested that reactivity against cathelicidins in arthritis is likely an epiphenomenon that results from extensive over-expression of the peptide in inflamed tissues[9]. In other words, it is incidental. Research in mouse models of arthritis indicate that peptides derived from LL-37 confer protection against collagen damage that often occurs in inflammatory arthritis. Administration of these peptides directly to affected joints decreases the severity of disease as well as serum levels of antibody against type II collagens[10]。この研究に基づいて、LL-37はおそらく関節炎において保護活性があると推測することは合理的です。この推測は、LL-37とその誘導体が、炎症性関節炎の重症度と直接関連する分子であるインターロイキン-32によって引き起こされる炎症を調節することが示されているという事実によって支持されています。[11]. Arthritis has also been associated with an up-regulation of toll-like receptor 3 in the fibroblasts of synovial fluid, a factor that likely aggravates arthritis by increasing inflammatory cytokine levels[12]。 LL-37は、TLR4に結合し、炎症誘発性または抗炎症効果を促進することが示されています。 TLR3のアップレギュレーションの設定では明らかではありませんが、研究は進行中です。 LL-37が過去に炎症誘発性マクロファージの反応を選択的に減少させることがわかっていることを考えると、炎症を選択的に減少させる可能性があるという考えは不合理ではありません[13].LL-37および腸
細胞培養の研究は、LL-37が腸にいくつかの効果があることを示しています。第一に、ペプチドは腸の上皮障壁を維持するために必要な細胞の移動を増加させます。第二に、LL-37は腸の炎症の環境でアポトーシスを減少させ、多くの炎症状態の病因を遅らせるのに役立ちます。全体として、この研究は、LL-37が腸の手術後、または急性腸感染症の環境における炎症性腸症状における有用なアジュバント治療である可能性があることを示しています。抗生物質療法のアジュバントとして役立つことさえあるかもしれません。[14]. LL-37 does not work alone in the intestine, pairing once again with human beta defensin 2 to promote wound healing. Research in cell culture indicates that the peptides work in tandem to both repair and maintain intestinal epithelium while reducing TNF-related cell death[15]。現在、TNF-alpha阻害剤は、炎症性腸状態の治療の主力です。それらは効果的な薬ですが、結核などの深刻な感染のリスクの劇的な増加を引き起こすなど、多くの深刻な副作用があります。炎症性腸疾患のLL-37ベースの治療法の開発は、TNF-α阻害剤への依存を減らし、この患者集団の罹患率と死亡率を改善するのに役立ちます。LL-37および腸がん
LL-37と癌に関する研究はさまざまな結果をもたらしましたが、ペプチドは、喫煙やタバコの使用に関連する口腔扁平上皮癌を含む腸および胃癌の環境で有益であると思われます。興味深いことに、これらの効果はビタミンD依存性経路によって媒介されるように見えます。これは、ビタミンの服用が以前にGIがんのリスクの低下と関連していた理由を説明するかもしれません。ビタミンDは、LL-37を介して腫瘍関連マクロファージの抗癌活性を誘発するように見えます[16].LL-37および血管の成長
LL-37は、内皮細胞のプロスタグランジンE2(PGE2)の合成を引き起こすようです。 PGE2は、炎症性疼痛と血管の成長の両方に関連していますが、これらの効果は分子が発現している場所によって異なります。内皮細胞では、PGE2は血管新生と呼ばれるプロセスで血管の発達を引き起こします[17]。これは、特定の設定に応じて、良い面と悪い面でも悪い場合があります。血管新生を調節する能力は、癌の発症、心臓病、脳卒中の結果、創傷治癒などに影響を与えるため、過去数十年に多くの研究の焦点でした。 LL-37活動は、血管新生経路を調査するための有用な手段を提供し、潜在的な将来の介入のモデルは、必要に応じて血管の成長を促進し(心臓病など)、有害な場合(癌など)に阻止します。進行中のLL-37研究
LL-37の興味深いことの1つは、他の哺乳類とは異なる構造があることです。[18]. These alternative structures result in different functions for the same basic peptide and provide insight into how three-dimensional configuration can impact receptor binding. This feature makes LL-37 of intense interest because it allows scientists to study the impacts of simple amino acid sequence changes on structure and ultimately function. This could inform an entire branch of biochemistry and make it easier for scientists to manipulate protein production to achieve very specific results.
LL-37 exhibits minimal to moderate side effects, low oral and excellent subcutaneous bioavailability in mice. Per kg dosage in mice does not scale to humans. LL-37 for sale at
ペプチドグル人間の消費ではなく、教育的および科学的研究のみに限定されています。あなたが認可された研究者である場合にのみ、LL-37を購入してください。
記事著者
Scientific Journalの著者
ダニエラ・ジンドリ博士トリエステ大学ユニット・ライフサイエンス省で事業を展開しています。彼女の焦点は、グラム陰性の細菌、炎症誘発性および抗膨張経路の同時に同時に調節するLL-37の生物学的活性、およびLL-37の抗菌および抗菌効果を取り囲んでいます。ダニエラ・ジンドリ博士LL-37の研究開発に関与する主要な科学者の一人として参照されています。この医師/科学者は、何らかの理由でこの製品の購入、販売、または使用を承認または提唱することは決してありません。関係や関係はありません。
ペプチドグルそしてこの医者。医師を引用する目的は、このペプチドを研究している科学者が実施した徹底的な研究開発努力を認め、認識し、称賛することです。DanielaXhindoli博士。参照された引用の下に[18]にリストされています。
参照された引用
- J. M. Kahlenberg and M. J. Kaplan, “Little peptide, big effects: the role of LL-37 in inflammation and autoimmune disease,” J. Immunol. Baltim. Md 1950, vol. 191, no. 10, Nov. 2013.
D. S. Alexandre-Ramos et al., “LL-37 treatment on human peripheral blood mononuclear cells modulates immune response and promotes regulatory T-cells generation,” Biomed. Pharmacother. Biomedecine Pharmacother., vol. 108, pp. 1584–1590, Dec. 2018.
P. Y. Ong et al., “Endogenous antimicrobial peptides and skin infections in atopic dermatitis,” N. Engl. J. Med., vol. 347, no. 15, pp. 1151–1160, Oct. 2002.
C. D. Ciornei, T. Sigurdardóttir, A. Schmidtchen, and M. Bodelsson, “Antimicrobial and chemoattractant activity, lipopolysaccharide neutralization, cytotoxicity, and inhibition by serum of analogs of human cathelicidin LL-37,” Antimicrob. Agents Chemother., vol. 49, no. 7, pp. 2845–2850, Jul. 2005.
X. Chen et al., “Synergistic effect of antibacterial agents human β-defensins, cathelicidin LL-37 and lysozyme against Staphylococcus aureus and Escherichia coli,” J. Dermatol. Sci., vol. 40, no. 2, pp. 123–132, Nov. 2005.
M. Golec, “Cathelicidin LL-37: LPS-neutralizing, pleiotropic peptide,” Ann. Agric. Environ. Med. AAEM, vol. 14, no. 1, pp. 1–4, 2007.
R. Shaykhiev et al., “Human endogenous antibiotic LL-37 stimulates airway epithelial cell proliferation and wound closure,” Am. J. Physiol. Lung Cell. Mol. Physiol., vol. 789, no. 5, pp. L842-848, Nov. 2005.
M. H. Hoffmann et al., “The cathelicidins LL-37 and rCRAMP are associated with pathogenic events of arthritis in humans and rats,” Ann. Rheum. Dis., vol. 72, no. 7, pp. 1239–1248, Jul. 2013.
D. Kienhöfer et al., “No evidence of pathogenic involvement of cathelicidins in patient cohorts and mouse models of lupus and arthritis,” PloS One, vol. 9, no. 12, p. e115474, 2014.
L. N. Y. Chow et al., “Human cathelicidin LL-37-derived peptide IG-19 confers protection in a murine model of collagen-induced arthritis,” Mol. Immunol., vol. 57, no. 2, pp. 86–92, Feb. 2014.
K.-Y. G. Choi, S. Napper, and N. Mookherjee, “Human cathelicidin LL-37 and its derivative IG-19 regulate interleukin-32-induced inflammation,” Immunology, vol. 143, no. 1, pp. 68–80, Sep. 2014.
W. Zhu et al., “Arthritis is associated with T-cell-induced upregulation of Toll-like receptor 3 on synovial fibroblasts,” Arthritis Res. Ther., vol. 13, no. 3, p. R103, Jun. 2011.
K. L. Brown et al., “Host defense peptide LL-37 selectively reduces proinflammatory macrophage responses,” J. Immunol. Baltim. Md 1950, vol. 186, no. 9, pp. 5497–5505, May 2011.
J.-M. Otte et al., “Effects of the cathelicidin LL-37 on intestinal epithelial barrier integrity,” Regul. Pept., vol. 156, no. 1–3, pp. 104–117, Aug. 2009.
J.-M. Otte et al., “Human beta defensin 2 promotes intestinal wound healing in vitro,” J. Cell. Biochem., vol. 104, no. 6, pp. 2286–2297, Aug. 2008.
X. Chen et al., “Roles and Mechanisms of Human Cathelicidin LL-37 in Cancer,” Cell. Physiol. Biochem. Int. J. Exp. Cell. Physiol. Biochem. Pharmacol., vol. 47, no. 3, pp. 1060–1073, 2018.
Salvado M. Dolores, Di Gennaro Antonio, Lindbom Lennart, Agerberth Birgitta, and Haeggström Jesper Z., “Cathelicidin LL-37 Induces Angiogenesis via PGE2–EP3 Signaling in Endothelial Cells, In Vivo Inhibition by Aspirin,” Arterioscler. Thromb. Vasc. Biol., vol. 33, no. 8, pp. 1965–1972, Aug. 2013.
D. Xhindoli, S. Pacor, M. Benincasa, M. Scocchi, R. Gennaro, and A. Tossi, “The human cathelicidin LL-37 — A pore-forming antibacterial peptide and host-cell modulator,” Biochim. Biophys. Acta BBA – Biomembr., vol. 1858, no. 3, pp. 546–566, Mar. 2016.